题目内容
17.下列物质中,只含极性共价键的化合物是( )| A. | H2O | B. | Cl2 | C. | NH4Cl | D. | NaOH |
分析 同种非金属元素之间形成非极性共价键,不同非金属元素之间形成极性共价键,以此来解答.
解答 解:A.水中只有O-H极性共价键,故A正确;
B.氯气中只有Cl-Cl非极性键,属于单质,故B错误;
C.NH4Cl中铵根离子与氯离子以离子键结合,N、H之间以极性共价键结合,则NH4Cl为含有极性共价键的离子化合物,故C错误;
D.NaOH中含有离子键和O-H极性键,属于化合物,故D错误.
故选A.
点评 本题考查化学键,明确元素的类别及元素的成键是解答本题的关键,难度较小.

练习册系列答案
相关题目
2.反应A+3B═2C+2D在四种不同的情况下的反应速率如下,最快的是( )
| A. | v(A)=0.15mol/(L•min) | B. | v(B)=0.6mol/(L•min) | ||
| C. | v(c)=0.4mol/(L•min) | D. | v(D)=0.45mol/(L•min) |
3.已知反应M+N=X+Y为吸热反应,对这个反应的下列说法正确的是( )
| A. | M的能量一定低于X的,N的能量一定低于Y的 | |
| B. | 因为该反应为吸热反应,故一定要加热反应才能进行 | |
| C. | 破坏反应物中化学键吸收的能量小于形成生成物中化学键所放出的能量 | |
| D. | M和N的总能量一定低于X和Y的总能量 |
12.热化学方程式中化学式前的系数表示的是( )
| A. | 分子个数 | B. | 原子个数 | C. | 物质的质量 | D. | 物质的量 |
2.下列气体中,不能用排空气法收集的是( )
| A. | NO | B. | SO2 | C. | CO2 | D. | NO2 |
9.下列关于钠及其化合物的叙述正确的是( )
| A. | Na和Na+的化学性质相似 | |
| B. | 钠在空气中燃烧生成氧化钠 | |
| C. | 钠可与硫酸铜溶液反应得到铜 | |
| D. | 实验室通常把钠保存在石蜡油或煤油中 |
6.设N0为阿伏加德罗常数的值,下列说法中正确的是( )
| A. | 18gH2O所含的电子数目为9N0 | |
| B. | 0.1 mol/L Na2SO4溶液所含Na+数目为0.2N0 | |
| C. | 1 mol钠完全反应时所失去的电子数为N0 | |
| D. | 标准状况下22.4L O2所含的原子数目为N0 |
7.用NA表示阿伏加德罗常数的值,下列说法正确的是( )
| A. | 0.1mol-NH2(氨基)中含有的电子数为0.7NA | |
| B. | 60gSiO2中含有NA个SiO2分子 | |
| C. | 7.8g由Na2S和Na2O2组成的混合物中含有阴离子的数目为0.1NA | |
| D. | 1molFe与1mol氯气反应转移3NA个电子 |
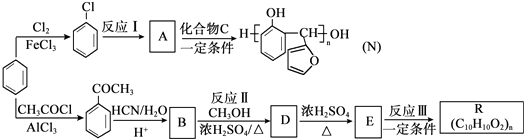

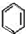 生成
生成 的反应类型是取代反应.
的反应类型是取代反应.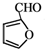 .
. .
.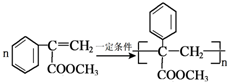 .
.