题目内容
12.臭氧在烟气脱硝中的反应为2NO2(g)+O3(g)?N2O5(g)+O2(g).若此反应在恒容密闭容器中进行,相关图象如下列选项,其中对应分析结论正确的是( )| A. | B. | C. | D. |
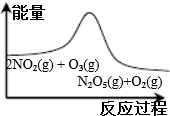 | 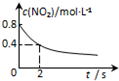 |  | 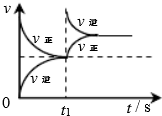 |
| 平衡后升温, NO2含量降低 | 0~2s内, v(O3)=0.2 mol•L-1•s-1 | V正:b点>a点 b点:v逆>v正 | 恒温,t1时再充入O3 |
| A. | A | B. | B | C. | C | D. | D |
分析 A.由图可知,反应物总能量高于生成物总能量,正反应为放热反应,升高温度平衡向逆反应方向移动;
B.由图可知,0-2s内,二氧化氮的浓度变化量=0.8mol/L-0.4mol/L=0.4mol/L,根据v=$\frac{△c}{△t}$计算v(NO2),然后依据化学计量数之比等于速率之比计算v(O3);
C.温度高,化学反应速率快,此反应为放热反应,温度升高,平衡左移;
D.容器中充入反应物,正反应速率瞬间加快,逆反应速率不变,据此解答即可.
解答 解:A.由图可知,反应物总能量高于生成物总能量,正反应为放热反应,升高温度平衡向逆反应方向移动,NO2的含量增大,故A错误;
B.由图可知,0-2s内,二氧化氮的浓度变化量=0.8mol/L-0.4mol/L=0.4mol/L,故v(NO2)=$\frac{0.4mol/L}{2s}$=0.2mol/(L.s),v(O3)=$\frac{1}{2}$v(NO2)=0.1mol/(L.s),故B错误;
C.度高,化学反应速率快,b点温度高于a点,故V正:b点>a点,此反应为放热反应,温度升高,平衡左移,故b点:v逆>v正,故C正确;
D.容器中充入反应物,正反应速率瞬间加快,逆反应速率不变,故D错误,故选C.
点评 本题以图象形式,考查化学反应中能量变化、化学反应速率计算、化学平衡图象及影响因素等,难度较大.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
12.下列事实和平衡移动无关的是( )
| A. | 开启啤酒后,瓶中立刻泛起大量泡沫 | |
| B. | 实验室中常用排饱和食盐水的方法收集Cl2 | |
| C. | 合成氨工业中不断分离出液氨有利于NH3的生成 | |
| D. | 氯化亚铁溶液久置呈黄色 |
20.下列说法正确的是( )
| A. | 氯化铵受热固体消失和干冰升华只需克服分子间作用力 | |
| B. | NaF、H2SO4中所含化学键类型相同 | |
| C. | HCl气体溶于水和NaOH熔化破坏的化学键类型相同 | |
| D. | I2、Br2、Cl2、F2 熔沸点逐渐降低 |
17.有机物蒽的结构简式为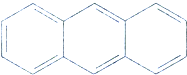 ,它的二溴代物的同分异构体的数目为( )
,它的二溴代物的同分异构体的数目为( )
 ,它的二溴代物的同分异构体的数目为( )
,它的二溴代物的同分异构体的数目为( )| A. | 13 | B. | 14 | C. | 15 | D. | 16 |
4.下列各组离子在溶液中能够大量共存的是( )
| A. | NH4+、Cl-、Na+、SO42- | B. | Na+、Ba2+、OH-、SO42- | ||
| C. | Ca2+、H+、S2-、ClO- | D. | H+、Cl-、Fe2+、NO3- |
1.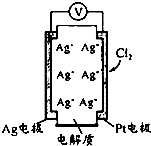 利用如图所示原电池可测量空气中Cl2含量,其中电解质是Ag+可以自由移动的固体物质.下列分析不正确的是( )
利用如图所示原电池可测量空气中Cl2含量,其中电解质是Ag+可以自由移动的固体物质.下列分析不正确的是( )
 利用如图所示原电池可测量空气中Cl2含量,其中电解质是Ag+可以自由移动的固体物质.下列分析不正确的是( )
利用如图所示原电池可测量空气中Cl2含量,其中电解质是Ag+可以自由移动的固体物质.下列分析不正确的是( )| A. | 电子经外电路流向Pt电极 | |
| B. | 正极反应:Cl2+2e-+2Ag+=2AgCl | |
| C. | 电池工作时,电解质中Ag+数目减少 | |
| D. | 空气中c(Cl2)越大,Ag极消耗速率越快 |
2.按下列路线制聚氯乙烯,未发生的反应类型是( )
C2H5Br→CH2=CH2→C1H2C-CH2Cl→CH2=CHCl→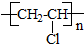
C2H5Br→CH2=CH2→C1H2C-CH2Cl→CH2=CHCl→
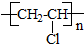
| A. | 消去反应 | B. | 取代反应 | C. | 加成反应 | D. | 加聚反应 |
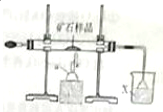 下面是模拟工业上隔绝空气条件下灼烧铜矿样品(主要成分为Cu2S和Cu2O的混合物)冶炼铜的实验装置图:
下面是模拟工业上隔绝空气条件下灼烧铜矿样品(主要成分为Cu2S和Cu2O的混合物)冶炼铜的实验装置图: