题目内容
5.氧化还原是一类重要的反应.(1)已知反应:①Cu+2Fe3+=Cu2++2Fe2+,②Cu2++Fe=Cu+Fe2+
两个反应中各种离子的氧化性从强到弱的顺序是Fe3+>Cu2+>Fe2+.
(2)在反应MnO2+4HCl$\frac{\underline{\;\;△\;\;}}{\;}$MnCl2+Cl2↑+2H2O中,当有0.2mol电子转移时,产生氯气的体积(标准状况)是2.24LL.
(3)已知反应:
3Cu+8HNO3(稀)=3Cu(NO3)2+2NO↑+4H2O
①该反应的氧化剂为HNO3,氧化产物为Cu(NO3)2;
②在该反应中稀硝酸所起的作用为氧化性和酸性;
③若反应中有0.15mol的铜参与反应,则被还原的硝酸的物质的量为0.1mol.
④用单线桥表示出反应中电子转移的方向和数目.
分析 (1)根据氧化还原反应反应中氧化剂氧化性大于氧化产物的氧化性,以此比较氧化性强弱;
(2)当有0.2mol电子转移时,生成0.1molCl2,以此可计算体积;
(3)①3Cu+8HNO3(稀)=3Cu(NO3)2+2NO↑+4H2O,N元素化合价降低,则硝酸为氧化剂,铜化合价升高,则铜为还原剂,生成Cu(NO3)2为氧化产物;
②3Cu+8HNO3(稀)=3Cu(NO3)2+2NO↑+4H2O,8mol硝酸参与反应,只有2mol化合价降低作氧化剂,其余作酸性;
③根据8mol硝酸参与反应,只有2mol化合价降低作氧化剂被还原判断;
④3Cu+8HNO3=3Cu(NO3)2+2NO+4H2O中,Cu元素的化合价由0升高为+2价,N元素的化合价由+5价降低为+4价,还原剂发生氧化反应,该反应中转移6e-,以此来解答.
解答 解:(1)由反应①可知氧化性Fe3+>Cu2+,由反应②可知氧化性Cu2+>Fe2+,则氧化性Fe3+>Cu2+>Fe2+,
故答案为:Fe3+>Cu2+>Fe2+;
(2)当有0.2mol电子转移时,生成0.1molCl2,标准状况下体积为2.24L,故答案为:2.24L;
(3)①由3Cu+8HNO3(稀)=3Cu(NO3)2+2NO↑+4H2O可知,N元素化合价降低,则HNO3为氧化剂,铜化合价升高,则铜为还原剂,生成Cu(NO3)2为氧化产物,
故答案为:HNO3;Cu(NO3)2;
②3Cu+8HNO3(稀)=3Cu(NO3)2+2NO↑+4H2O,8mol硝酸参与反应,只有2mol化合价降低作氧化剂,其余作酸性,所以稀硝酸所起的作用为氧化性和酸性,故答案为:氧化性和酸性;
③因为8mol硝酸参与反应,只有2mol化合价降低作氧化剂被还原,所以有0.15mol的铜参与反应,则被还原的硝酸的物质的量为0.15×$\frac{2}{3}$=0.1mol,故答案为:0.1;
④3Cu+8HNO3=3Cu(NO3)2+2NO+4H2O中,Cu元素的化合价由0升高为+2价,N元素的化合价由+5价降低为+4价,该反应中转移6e-,所以单线桥表示反应的电子转移的方向和数目 ,
,
故答案为: .
.
点评 本题考查氧化还原反应,侧重于概念的理解和计算,为高考高频考点,注意从元素化合价的角度认识氧化还原反应的相关概念和物质的性质,题目难度不大.

| A. | NaHSO4 | B. | Al2O3 | C. | NaHCO3 | D. | Al(OH)3 |
| A. | A和B分子中碳原子个数一定相同 | B. | A和B不可能是同系物 | ||
| C. | A和B中氢元素质量分数一定相同 | D. | A和B的化学性质一定相似 |
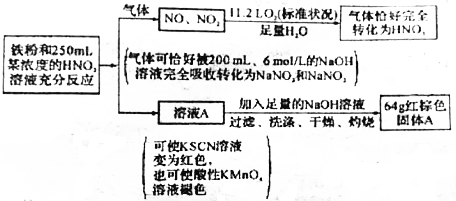
| A. | 原溶液中投入铁粉物质的量是0.25mo1 | |
| B. | 原溶液中HNO3的浓度是2.0mol•L-1 | |
| C. | 反应后的溶液中还可溶解9.6g铜 | |
| D. | 反应后的溶液中c(Fe2+):c(Fe3+)=3:1 |
| A. | 把金属铁放入稀硫酸中:Fe+2H+═Fe3++H2↑ | |
| B. | 往碳酸镁中滴加稀盐酸:CO32-+2H+═CO2↑+H2O | |
| C. | 向氢氧化铜中滴加稀盐酸:Cu(OH)2+2H+═Cu2++2H2O | |
| D. | 氢氧化钡溶液与稀硫酸反应:Ba2++SO42-+H++OH-═BaSO4↓+H2O |
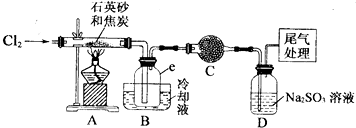
实验过程中;石英砂中的铁、铝等杂质也能转化为相应氯化物,SiCl4,A1C13,FeC13遇水均易水解,有关物质的物理常数见下表:
| 物质 | SiCl4 | AlCl3 | FeCl3 |
| 沸点/℃ | 57.7 | 315 | |
| 熔点/℃ | -70.0 | ||
| 升华温度/℃ | 180 | 300 |
(I)实验室制备氯气有以下五步操作,其正确操作顺序为④③⑤②①(填标号).
①向烧瓶中装入二氧化锰固体,向分液漏斗中加入浓盐酸
②检查装置的气密性
③把酒精灯放在铁架台上,根据酒精灯火焰确定铁圈高度,固定铁圈,放上石棉网
④在烧瓶上装好分液漏斗,安装好导气管
⑤将烧瓶固定在铁架台上
(2)装置A的硬质玻璃管中发生主要反应的化学方程式是2C+SiO2+2Cl2$\frac{\underline{\;高温\;}}{\;}$SiCl4+2CO↑
置A.B间导管短且粗的原因是防止生成物的AlCl3、FeCl3等杂质凝结成固体堵塞导管
验中尾气处理的方法是连接一个加热的装有CuO粉末的反应管
(3)装置B中e瓶收集到的粗产物可通过精馏(类似多次蒸馏)得到高纯度四氛化硅.在精馏过程中,不可能用到的仪器有CD(填正确答案标号).
A.圆底烧瓶 B.温度计 C.吸滤瓶 D球形冷凝管 E.接收器
(4)装置D中的Na2S03的作用主要是吸收未反应完的Cl2请设计一个实验,证明装置D中的Na2S03已被氧化(简述实验步骤):取少量溶液置于洁净的试管中,向其中滴加稀盐酸至不再产生气体(1分),再向其中滴入氯化钡溶液,若产生白色沉淀,证明亚硫酸钠被氧化
(5)SiCl4极易水解,其完全水解的产物为H4SiO4(或H2SiO3)和HCl.H2还原SiCl4制得高纯硅的过程中若混入O2,可能引起的后果是可能引起爆炸、硅被氧化得不到高纯硅.
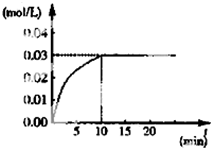 在某一容积为5L的体积不变的密闭容器内,加入 0.3mol的CO和0.3mol的H2O,在催化剂存在和800℃的条件下加热,发生如下反应:CO(g)+H2O(g)?CO2(g)+H2(g)△H>0,反应中CO2的浓度随时间变化情况如图:
在某一容积为5L的体积不变的密闭容器内,加入 0.3mol的CO和0.3mol的H2O,在催化剂存在和800℃的条件下加热,发生如下反应:CO(g)+H2O(g)?CO2(g)+H2(g)△H>0,反应中CO2的浓度随时间变化情况如图: