题目内容
3.能与Na反应放出H2,又能是溴水褪色,但不能使石蕊试纸变红色的物质是( )| A. | CH3-CH2-COOH | B. | CH2=CH-CH2-OH | C. | CH2=CH-COOH | D. | CH2=CH-COOCH3 |
分析 能与钠反应放出氢气,说明含有羟基或羧基,能与溴水反应,含有不饱和键,不能能使石蕊试纸变红色,说明不含羧基,以此解答该题.
解答 解:题中涉及物质中,能与钠反应放出氢气,说明含有羟基或羧基,能与溴水反应,含有不饱和键,不能能使石蕊试纸变红色,说明不含羧基,只有B符合.
故选B.
点评 本题考查有机物的结构与性质,为高频考点,把握官能团与性质的关系为解答的关键,侧重有机物性质及分析与应用能力的考查,题目难度不大.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
14.下列各组物质中,按酸、碱、盐、碱性氧化物、酸性氧化物的顺序排列正确的是( )
| A. | 盐酸、纯碱、氣酸钾、氧化镁、二氧化硅 | |
| B. | 硝酸、烧碱、次氯酸钠、氧化钙、二氧化硫 | |
| C. | 次氯酸、消石灰、硫酸铵、过氧化钠、二氧化碳 | |
| D. | 氨基酸、过氧化钠、碱式碳酸铜、氧化铁、一氧化碳 |
11.有一包白色固体(一种二元酸的正盐),下表为进行相关实验的部分实验报告.
(1)请根据实验现象,将你作出的判断填在表格内的相应位置.
(2)若想确认此白色固体的成分,应在步骤②(填步骤序号)中加入试剂A,试剂A为盐酸.
(3)在此实验中所使用仪器为普通玻璃,其组成可以用氧化物的形式来表示:Na2O•CaO•6SiO2,制造这种玻璃的原料是石灰石、纯碱和石英.若每天要生产10t玻璃,石灰石的利用率为80%计算,纯碱和石英的利用率按95%计算,每天至少需要纯碱和石灰石的质量是多少?(写出计算过程,计算结果保留两位有效数字)
(1)请根据实验现象,将你作出的判断填在表格内的相应位置.
| 步骤序号 | 操作 | 实验现象 | 判 断 |
| ① | 取固体溶于水,得溶液X | 得到无色溶液 | |
| ② | 取少量溶液X,加入氯化钡溶液 | 生成白色沉淀 | 可能含有SO42-、SO32-、CO32- (填离子符号) |
| ③ | 取少量溶液X,加入浓氢氧化钠溶液,加热,并在试管口用湿润的红色石蕊试纸检验 | 试纸变蓝 | 含有NH4+ (填离子符号) |
| 结论:此白色固体可能是(NH4)2SO4或(NH4)2SO3或(NH4)2CO3. | |||
(3)在此实验中所使用仪器为普通玻璃,其组成可以用氧化物的形式来表示:Na2O•CaO•6SiO2,制造这种玻璃的原料是石灰石、纯碱和石英.若每天要生产10t玻璃,石灰石的利用率为80%计算,纯碱和石英的利用率按95%计算,每天至少需要纯碱和石灰石的质量是多少?(写出计算过程,计算结果保留两位有效数字)
12.下列说法正确的是( )
| A. | CH2=CH2和CH3CH2Cl都属于烃 | B. | 乙烯和乙烷都能发生加聚反应 | ||
| C. | C3H6有三种同分异构体 | D. | 苯的硝化反应属于取代反应 |
10.化学与生产、生活密切相关,下列说法中正确的是( )
| A. | 高纯度的硅单质广泛用于制作光导纤维 | |
| B. | 在汽车排气管上加装尾气“催化转化器”可以有效减少有害气体的排放 | |
| C. | 气象环境报告中新增的“PM2.5”是对一种新分子的描述 | |
| D. | 为防止食品氧化变质,食品袋中放有硅胶包 |

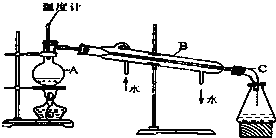 如图是某学生绘制的实验室蒸馏石油的装置图:
如图是某学生绘制的实验室蒸馏石油的装置图: