题目内容
【题目】苯甲酸乙酯是重要的精细化工试剂,常用于配制水果型食用香精。实验室制备流程如图:
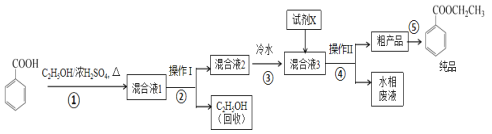
试剂相关性质如下表:
苯甲酸 | 乙醇 | 苯甲酸乙酯 | |
常温性状 | 白色针状晶体 | 无色液体 | 无色透明液体 |
沸点/℃ | 249.0 | 78.0 | 212.6 |
相对分子量 | 122 | 46 | 150 |
溶解性 | 微溶于水,易溶于乙醇、乙醚等有机溶剂 | 与水任意比互溶 | 难溶于冷水,微溶于热水,易溶于乙醇和乙醚 |
回答下列问题:
(1)为提高原料苯甲酸的纯度,可采用的纯化方法为__。
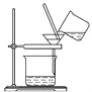
(2)步骤①的装置如图所示(加热和夹持装置已略去),将一小团棉花放入仪器B中靠近活塞孔处,将吸水剂(无水硫酸铜的乙醇饱和溶液)放入仪器B中,在仪器C中加入12.2g纯化后的苯甲酸晶体,30mL无水乙醇(约0.5mol)和3mL浓硫酸,加入沸石,加热至微沸,回流反应1.5~2h。仪器A的作用是__。

(3)随着反应进行,反应体系中水分不断被有效分离,仪器B中吸水剂的现象为__。
(4)反应结束后,对C中混合液进行分离提纯,操作I是_;操作II所用的玻璃仪器除了烧杯外还有__。
(5)反应结束后,步骤③中将反应液倒入冷水的目的除了溶解乙醇外,还有__;加入试剂X为___(填写化学式)。
(6)最终得到产物纯品10.0g,实验产率为__%(保留三位有效数字)。
【答案】重结晶 冷凝回流乙醇和水 吸水剂由白色变为蓝 蒸馏 分液漏斗 降低苯甲酸乙酯的溶解度,利于分层 Na2CO3或NaHCO3 66.7
【解析】
苯甲酸与乙醇在浓硫酸作催化剂发生酯化反应生成苯甲酸乙酯,苯甲酸乙酯与乙醇和苯甲酸能够混溶,苯甲酸乙酯与乙醇沸点差异较大,因此操作I为蒸馏,混合液2中主要成分为苯甲酸乙酯和苯甲酸,加入试剂X除去苯甲酸,因此可选择试剂饱和碳酸钠进行除杂,然后分液制备粗产品,然后通过干燥制备苯甲酸乙酯纯品,以此解答本题。
(1)可通过重结晶的方式提高原料苯甲酸的纯度,故答案为:重结晶;
(2)仪器A为球形冷凝管,在制备过程中乙醇易挥发,因此通过球形冷凝管冷凝回流乙醇和水,该反应中乙醇作为反应物,因此可通过水浴加热,避免乙醇大量挥发,故答案为:冷凝回流乙醇和水;
(3)仪器B中吸水剂为无水硫酸铜的乙醇饱和溶液,吸收水分后生成五水硫酸铜,吸水剂由白色变为蓝色,故答案为:吸水剂由白色变为蓝色;
(4)苯甲酸乙酯与乙醇和苯甲酸能够混溶,苯甲酸乙酯与乙醇沸点差异较大,因此操作I为蒸馏,混合液2中主要成分为苯甲酸乙酯和苯甲酸,加入试剂X除去苯甲酸,因此可选择试剂饱和碳酸钠进行除杂,然后分液制备粗产品,操作II为分液,除烧杯外,还需要的玻璃仪器为分液漏斗,故答案为:蒸馏;分液漏斗;
(5)因苯甲酸乙酯难溶于冷水,步骤③中将反应液倒入冷水的目的还有降低苯甲酸乙酯的溶解度有利于分层,混合液2中主要成分为苯甲酸乙酯和苯甲酸,加入试剂X除去苯甲酸,因此可选择试剂Na2CO3溶液或NaHCO3溶液进行除杂,故答案为:降低苯甲酸乙酯的溶解度,利于分层;Na2CO3或NaHCO3;
(6)12.2g苯甲酸的物质的量为![]() ,反应过程中乙醇过量,理论上产生苯甲酸乙酯的物质的量为0.1mol,质量为0.1mol×150g/mol=15g,实验产率为
,反应过程中乙醇过量,理论上产生苯甲酸乙酯的物质的量为0.1mol,质量为0.1mol×150g/mol=15g,实验产率为![]() ,故答案为:66.7。
,故答案为:66.7。

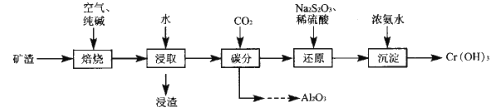
【题目】钴酸锂(LiCoO2)电池是一种应用广泛的新型电源,电池中含有少量的铝、铁、碳等单质。实验室尝试对废旧钴酸锂电池回收再利用。实验过程如下:
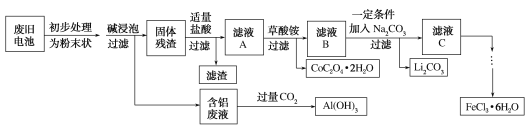
已知:①还原性:Cl->Co2+;
②Fe3+和![]() 结合生成较稳定的[Fe(C2O4)3]3-,在强酸性条件下分解重新生成Fe3+。回答下列问题:
结合生成较稳定的[Fe(C2O4)3]3-,在强酸性条件下分解重新生成Fe3+。回答下列问题:
(1)废旧电池初步处理为粉末状的目的是________。
(2)从含铝废液得到Al(OH)3的离子方程式为___________
(3)滤液A中的溶质除HCl、LiCl外还有________(填化学式)。写出LiCoO2和盐酸反应的化学方程式____________
(4)滤渣的主要成分为_______(填化学式)。
(5)在空气中加热一定质量的CoC2O4·2H2O固体样品时,其固体失重率数据见下表,请补充完整表中问题。
已知:①CoC2O4在空气中加热时的气体产物为CO2。
②固体失重率=对应温度下样品失重的质量/样品的初始质量。
序号 | 温度范围/℃ | 化学方程式 | 固体失重率 |
Ⅰ | 120~220 | CoC2O4·2H2O CoC2O4+2H2O | 19.67% |
Ⅱ | 300~350 | ______ | 59.02% |
(6)已知Li2CO3的溶度积常数Ksp=8.64×10-4,将浓度为0.02 mol·L-1的Li2SO4和浓度为0.02 mol·L-1的Na2CO3溶液等体积混合,则溶液中的Li+浓度为________ mol·L-1。