题目内容
2.有机物X的键线式为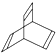 ,下列说法不正确的是( )
,下列说法不正确的是( )| A. | X的化学式为C8H8 | |
| B. | X能使高锰酸钾酸性溶液褪色 | |
| C. | 有机物Y是X的同分异构体,且属于芳香烃,则Y的结构简式为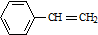 | |
| D. | X与足量的H2在一定条件下反应可生成环状的饱和烃Z,Z的一氯代物有4种 |
分析 A.键线式中交点为碳原子,用H原子饱和碳的四价结构;
B.X含有碳碳双键,具有烯烃的性质;
C.有机物Y是X的同分异构体,且属于芳香烃,则Y为苯乙烯;
D.X与足量的H2在一定条件下反应可生成环状的饱和烃Z,Z的分子中有2种H原子.
解答 解:A.由X的键线式可知,分子中有8个C原子、8个H原子,故其分子式为C8H8,故A正确;
B.X含有碳碳双键,能使高锰酸钾酸性溶液褪色,故B正确;
C.有机物Y是X的同分异构体,且属于芳香烃,则Y为苯乙烯,则Y的结构简式为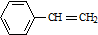 ,故C正确;
,故C正确;
D.X与足量的H2在一定条件下反应可生成环状的饱和烃Z,Z的分子中有2种H原子,Z的一氯代物有2种,故D错误,
故选:D.
点评 本题考查有机物的结构与性质,涉及键线式、烯烃性质、同分异构体等,难度不大,有利于基础知识的巩固.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
13. 离子交换膜法电解食盐水的示意如图,图中离子交换膜只允许阳离子通过.下列说法正确的是( )
离子交换膜法电解食盐水的示意如图,图中离子交换膜只允许阳离子通过.下列说法正确的是( )
 离子交换膜法电解食盐水的示意如图,图中离子交换膜只允许阳离子通过.下列说法正确的是( )
离子交换膜法电解食盐水的示意如图,图中离子交换膜只允许阳离子通过.下列说法正确的是( )| A. | e电极与电源的负极相连 | |
| B. | H+在f电极上发生还原反应 | |
| C. | 精制饱和食盐水从图中b位置补充 | |
| D. | 离子交换膜的作用只是防止生成的Cl2与H2发生反应 |
10.下列指定反应的离子方程式正确的是( )
| A. | 氯气溶于水:Cl2+H2O═2H++Cl-+ClO- | |
| B. | FeSO4溶液与氨水反应的离子方程式:Fe2++2NH3•H2O═Fe(OH)2↓+2NH4+ | |
| C. | 酸性溶液中KIO3与KI反应生成I2:I+I-+6H+═I2+3H2O | |
| D. | NaHCO3溶液中加足量Ba(OH)2溶液:2HCO3-+Ba2++2OH-═BaCO3↓+2H2O+CO2↑ |
17.下列各式中,属于正确的电离方程式的是( )
| A. | HCO${\;}_{3}^{-}$═CO${\;}_{3}^{2-}$+H+ | B. | NaHSO4═Na++HSO4- | ||
| C. | H3PO4?3H++PO${\;}_{4}^{3-}$ | D. | NH3•H2O?NH${\;}_{4}^{+}$+OH- |
7.0.2mol Na${\;}_{2}^{18}$O2与足量CO2完全反应后,下表对生成物Na2CO3 和O2的描述中正确的是( )
| Na2CO3的质量 | 关于O2的描述 | |
| A | 21.2g | O2的摩尔质量是36g•mol-1 |
| B | 21.6g | 生成标准状况下O2的体积为2.24L |
| C | 21.6g | O2的摩尔质量是34g•mol-1 |
| D | 22.4g | 生成标准状况下O2的体积为2.24L |
| A. | A | B. | B | C. | C | D. | D |
11.配制一定物质的量浓度的NaOH溶液,下面描述正确的是( )
| A. | 用托盘天平称取25.20gNaOH | |
| B. | 将称好的NaOH固体放入容量瓶中加入少量水溶解 | |
| C. | 未冷却就将烧杯中的NaOH溶液注入容量瓶中会导致溶液浓度偏高 | |
| D. | 定容时,液面超过了容量瓶刻度线,用胶头滴管吸出刻度线以上的溶液 |
12.在一定条件下,2SO2(g)+O2(g)?2SO3(g)+Q(Q>0)反应已达到平衡,若保持其他条件不变,升高反应体系温度,则下列说法错误的是( )
| A. | 正、逆反应速率都增大 | B. | 正反应速率减小,逆反应速率增大 | ||
| C. | 平衡向逆反应方向移动 | D. | 混合气体中SO2的体积百分数增大 |