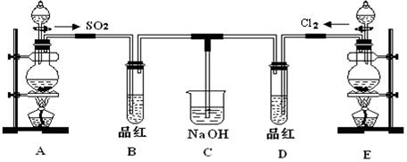
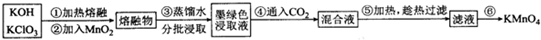��Ŀ����
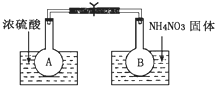
12�����ʵ����ͺ���Ԫ�صĻ��ϼ����о��������ʵ�������Ҫ�ӽǣ����仯�������̬�仯Ϊ����Ķ�άת����ϵ��ͼ1��ʾ�����������գ�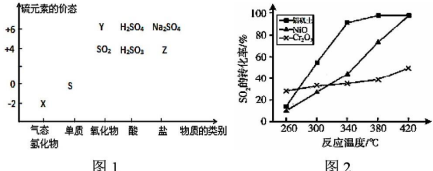
��1��ͼ1��X��ˮ��Һ�ڿ����з����ױ���ǣ�д����Ӧ�Ļ�ѧ����ʽ��2H2S+O2=2S��+2H2O��
��2��������������Na2S203�Ʊ�����������ԭ��Ӧ�ĽǶȷ������������п���ʵ�ֵķ����ǣ�ѡ���ţ�bd��
a��Na2S+S b��Z+S C��Na2S03+Y d��NaHS+NaHS03
��3���벹���������������Ļ�ѧ����ʽ��
4KAl��SO4��2.12H2O+3S�T2K2SO4+2Al2O3+9SO2��+48H2O
��4���о���ӦNa2S2O3+H2SO4=Na2SO4+S+SO2+H20������ʱ�����з�����������b��
a���ⶨһ��ʱ��������S02��������ó��÷�Ӧ������
b���о�Ũ�ȡ��¶ȵ����ضԸ÷�Ӧ���ʵ�Ӱ�죬�ȽϷ�Ӧ���ֻ��ǵ�ʱ��
c����Na2S2O3��S���ֱ���Ũ��ϡ���ᷴӦ���о�Ũ�ȶԸ÷�Ӧ���ʵ�Ӱ��
��5��������CO��SO2���̵�����������������������CO��SO2��380��ʱת��ΪS��һ�������壮��֪��
������۵㣺112.8�桢�е㣺444.6�棻
�ڷ�Ӧÿ�õ�Imol�ų�270kJ��������д���������̵�����Ӧ���Ȼ�ѧ����ʽ2CO��g��+SO2��g��=S��l��+2CO2 ��g����H=-270kJ/mol��
��һ�������£���CO��SO2�������Ϊ4��1���ں����ܱ������з���������Ӧ������ѡ����˵����Ӧ�ﵽƽ��״̬����cd����д��ĸ��ţ���
a��v ��CO����v��SO2��=2��1 b��ƽ�ⳣ������
c�������ܶȲ��� d��C02��S02������ȱ��ֲ���
���������Ӧ��ƽ��ʱ�����������CO���������Ϊ$\frac{7}{11}$����SO2��ת����Ϊ60%��
��6������������ͬ��������ͬʱ��������Ӧ��SO2��ת�����淴Ӧ�¶ȵı仯��ͼ2�������Ǵ����۸����أ�������ѡ����������������Ҫԭ����������������������Խϵ��¶��£���λʱ���ڻ�ýϸߵ�SO2ת���ʣ��ܺ�С��
���� ��1��XΪH2S��H2S�ڿ����б��������Ϊ����������ΪS��
��2��Na2S2O3��SΪ+2�ۣ���������ԭ�ĽǶȷ�������Ӧ����SԪ�ػ��ϼ۱���ֱ����2��С��2��
��3����ԭ�Ӻ�Ԫ���غ��֪��ȱ��Ϊˮ����ϵ��ӡ�ԭ���غ���ƽ��
��4�������������ϡ���ᷴӦ�����˵�������Һ����ǣ���Ӧ����Խ�죬���ֻ���ʱ��Խ�̣�
��5���ڷ�Ӧÿ�õ�1mol�ų�270kJ���������Դ���д�Ȼ�ѧ����ʽ���۷�Ӧ�ﵽƽ��״̬ʱ���淴Ӧ������ȣ������Ũ�ȱ��ֲ��䣬�ݴ˷�������������ʽ��������������ת���ʣ�
��6����ͼ��֪����ͬ������������������ʱ�����������ת�������
��� �⣺��1��XΪH2S��H2S�ڿ����б��������Ϊ����������ΪS����Ӧ�Ļ�ѧ����ʽΪ2H2S+O2=2S��+2H2O��
�ʴ�Ϊ��2H2S+O2=2S��+2H2O��
��2��Na2S2O3��SΪ+2�ۣ���������ԭ�ĽǶȷ�������Ӧ����SԪ�ػ��ϼ۱���ֱ����2��С��2��a��S���ϼ۶�С��2��c��S�Ļ��ϼ۶�����2��bd�������⣬
�ʴ�Ϊ��bd��
��3����ԭ�Ӻ�Ԫ���غ��֪��ȱ��Ϊˮ����Ӧ��SԪ�صĻ��ϼ���+6�۽���Ϊ+4�ۣ�SԪ�صĻ��ϼ���0����Ϊ+4�ۣ���ϵ��ӡ�ԭ���غ��֪��ӦΪ4KAl��SO4��2•12H2O+3S$\frac{\underline{\;����\;}}{\;}$2K2SO4+2Al2O3+9SO2��+48H2O��
�ʴ�Ϊ��4��3��2��2��9��48H2O��
��4�����������������ϡ���ᷴӦ�����˵�������Һ����ǣ������жϷ�Ӧ���ʿ�������Ӧ����Խ�죬���ֻ���ʱ��Խ�̣�
�ʴ�Ϊ��b��
��5���ڷ�Ӧÿ�õ�1mol�ų�270kJ���������Ȼ�ѧ����ʽΪ2CO��g��+SO2��g��=S��l��+2CO2 ��g����H=-270kJ/mol��
�ʴ�Ϊ��2CO��g��+SO2��g��=S��l��+2CO2 ��g����H=-270kJ/mol��
��a��CO��SO2������֮��ʼ�յ��ڻ�ѧ������֮�ȣ������жϷ�Ӧ�Ƿ�ﵽƽ��״̬����a����
b���¶Ȳ���ƽ�ⳣ��ʼ�ղ��䣬ƽ�ⳣ�����䲻��˵����Ӧ�ﵽƽ��״̬����b����
c������������䣬SΪ��̬����Ӧ����������������С����������������ʱ��˵�������Ũ�Ȳ��䣬��Ӧ�ﵽƽ��״̬����c��ȷ��
d��CO2��SO2������ȱ��ֲ���˵�����淴Ӧ������ȣ���Ӧ�ﵽƽ��״̬����d��ȷ��
�� 2CO��g��+SO2 ��g���TS��s��+2CO2��g��
��Ӧǰ��mol�� 4 1 0 0
ת���ˣ�mol�� 2x x x 2x
ƽ���mol�� 4-2x 1-x x 2x
���������CO���������Ϊ$\frac{7}{11}$������$\frac{4-2x}{4-2x+1-x+2x}$=$\frac{7}{11}$��x=0.6��
����SO2��ת����Ϊ$\frac{0.6}{1}$��100%=60%��
�ʴ�Ϊ��cd��60%��
��6����ͼ��֪��������ѡ����������������Ҫԭ����������������������Խϵ��¶��£���λʱ���ڻ�ýϸߵ�SO2ת���ʣ��ܺ�С��
�ʴ�Ϊ��������������������Խϵ��¶��£���λʱ���ڻ�ýϸߵ�SO2ת���ʣ��ܺ�С��
���� ���⿼����ۺϣ��漰�ǽ����ԱȽϡ�������ԭ��Ӧ����Ӧ���ʼ��Ȼ�ѧ����ʽ����ѧƽ��״̬���жϡ�ת���ʼ���ȣ����ط�Ӧԭ���и�Ƶ����Ŀ��飬�ۺ��Խ�ǿ����Ŀ�Ѷ��еȣ�

 �Ķ��쳵ϵ�д�
�Ķ��쳵ϵ�д�| A�� | Cu����ϡHNO3��3Cu+2NO${\;}_{3}^{-}$+8H+�T3Cu2++2NO��+4H2O | |
| B�� | ��NH4��2Fe��SO4��2��Һ�����NaOH��Һ��Ӧ��Fe��OH��2��Fe2++2OH-�TFe��OH��2�� | |
| C�� | ��CH3COOH�ܽ�CaCO3��CaCO3+2H+�TCa2++H2O+CO2�� | |
| D�� | AlCl3��Һ�м������ϡ��ˮ��Al3++4NH3•H2O�TAlO${\;}_{2}^{-}$+4NH${\;}_{4}^{+}$+2H2O |
| A�� | ������������������ɴ�ߡ�����ҩ����� | |
| B�� | ���ơ��������Ƚ���Ԫ�ص�������Ѥ������ɫ��������������� | |
| C�� | �����������ڱ걾��������������ʹ�����ʱ��Ե����� | |
| D�� | ����������ʱ������84����Һ���ܻ��ã�������ܷ����ж����� |
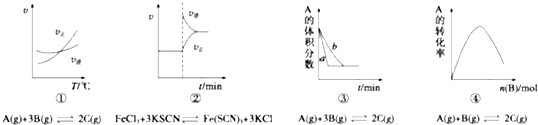
| A�� | ������������һ��ʱ����Ӧ�������¶ȱ仯��ͼ��������Ӧ��H��0 | |
| B�� | ������ƽ����ϵ����Һ����������KCl�����ѧ��Ӧ������ʱ��仯��ͼ�� | |
| C�� | ���������������������£�����ƽ����̵�ͼ��b��ʹ�ô���ʱ������ | |
| D�� | ����һ�������£�����һ����A�ĺ����ܱ�����������B����ƽ��ʱA��ת���ʵ�ͼ�� |
 ��֪2NO2��g���TN2O4��g����H��298K��=-52.7kJ•mol-1��ij����С��Ϊ��̽���¶Ⱥ�ѹǿ�Ի�ѧƽ���Ӱ�죬������������ʵ�飺
��֪2NO2��g���TN2O4��g����H��298K��=-52.7kJ•mol-1��ij����С��Ϊ��̽���¶Ⱥ�ѹǿ�Ի�ѧƽ���Ӱ�죬������������ʵ�飺