题目内容
【题目】个化学反应,我们不但关心物质变化和能量变化,还通常要研究化学反应的快慢

(1)用纯净的锌粒和盐酸反应制取氢气,回答:
实验过程如下图所示,分析判断:________段化学反应速率最快,原因是___________________,_______段收集的氢气最多。
为了加快上述反应的速率,欲向溶液中加入一定量下列物质,你认为可行的是________
A.胆矾晶体 B.硫酸氢钠固体
C.氯化锌浓溶液 D.浓硝酸
除了上述方法外,你认为还可以采取____________________措施来加快化学反应速率。
(2)下图表示800℃时,A、B、C三种气体物质的浓度随时间变化的情况,t是达到平衡状态的时间。
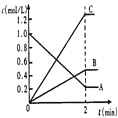
试回答
①该反应的化学方程式为_________________________________。
②达到平衡状态的所需时间是2min,A物质的平均化学反应速率为_______________
【答案】EF 反应放热,溶液温度升高,反应速率加快 EF AB 加热或把锌处理成小颗粒 2A![]() B+3C 0.4mol/(L·min)
B+3C 0.4mol/(L·min)
【解析】
(1)反应速率越快,则曲线的斜率越大,所以根据图像可知,EF段反应速率最快。这是由于反应放热,溶液温度升高,反应速率加快;根据纵坐标的变化可知,EF 段产生的氢气最多;胆矾溶于水,锌能置换出铜,从而构成铜锌原电池,加快反应速率,A正确;硫酸氢钠溶于水电离出氢离子,增大氢离子浓度,反应速率加快,B正确;氯化锌的浓溶液不能改变氢离子的浓度,反应速率变化不大,C错误;硝酸是氧化性酸,和锌反应得不到氢气,D不正确,答案选AB;由于温度和固体的表面积也可以改变反应速率,所以加热或把锌处理成小颗粒;施来加快化学反应速率。
(2)①根据图像可知,反应进行到2min时物质的浓度不再发生变化,反应达到平衡状态。其中A的浓度减少了0.8mol/L,B和C的浓度分别增加了0.4mol/L和1.2mol/L,则根据变化量之比是化学计量数之比可知,该反应的方程式是2A![]() B+3C。
B+3C。
②平衡时A的反应速率是0.8mol/L÷2min=0.4 mol/(L·min)。

【题目】在一定温度下,将气体X和气体Y各0.16mol充入10L恒容密闭容器中,发生反应
X(g)+Y(g) ![]() 2Z(g) △H < 0,一段时间后达到平衡,反应过程中测定的数据如下表:
2Z(g) △H < 0,一段时间后达到平衡,反应过程中测定的数据如下表:
t/min | 2 | 4 | 7 | 9 |
n(Y)/mol | 0.12 | 0.11 | 0.10 | 0.10 |
下列说法正确的是
A.反应前2min的平均速率ν(Z)=2.0×10-3mol·L-1·min-1
B.其他条件不变,降低温度,反应达到新平衡前ν(逆)> ν(正)
C.该温度下此反应的平衡常数K=1.44
D. 其他条件不变,再充入0.2molZ,平衡时X的体积分数增大
【题目】现有部分元素的性质与原子![]() 或分子
或分子![]() 结构如表所示:
结构如表所示:
元素编号 | 元素性质与原子 |
T | 最外层电子数是次外层电子数的3倍 |
X | 常温下单质分子为双原子分子,分子中含有3对共用电子对 |
Y | M层比K层少1个电子 |
Z | 第三周期元素的金属离子中半径最小 |
(1)画出元素T的原子结构示意图:__。
(2)元素Y与元素Z相比,金属性较强的是__![]() 用元素符号表示
用元素符号表示![]() ,下列表述中能证明这一事实的是___
,下列表述中能证明这一事实的是___![]() 填字母
填字母![]() 。
。
a.Y单质的熔点比Z单质低
b.Y的化合价比Z低
c.Y单质与水反应比Z单质与水反应剧烈
d.Y最高价氧化物对应的水化物的碱性比Z的强
(3)T、X、Y、Z中的两种元素能形成既有离子键又有非极性共价键的化合物,写出该化合物的化学式:__。
(4)T可以形成稳定的阴离子Tm-,Y可以形成稳定的阳离子Yn+,其半径关系为r(Tm-)__r(Yn+)(填“>”,“<”或“=”)
(5)X、Y、Z的最高价氧化物对应的水化物可以相互发生反应,写出Y、Z的最高价氧化物对应的水化物之间反应的离子方程式___。