题目内容
【题目】将一定量的氯气通入![]() 的氢氧化钠浓溶液中,加热少许时间后,溶液中形成NaCl、NaClO、
的氢氧化钠浓溶液中,加热少许时间后,溶液中形成NaCl、NaClO、![]() 共存体系(不考虑氯气和水的反应)。下列说法正确的是
共存体系(不考虑氯气和水的反应)。下列说法正确的是
A.若反应中转移的电子为n mol,则![]()
B.溶液中![]() 可能为
可能为![]()
C.与NaOH反应的氯气物质的量:![]()
D.当溶液中![]() 时,反应的离子方程式为:
时,反应的离子方程式为:![]()
【答案】D
【解析】
![]() ,则
,则
A.氯气和NaOH反应有![]() 、
、![]() ,当生成NaCl和NaClO时转移电子最少,
,当生成NaCl和NaClO时转移电子最少,![]() 消耗
消耗![]() ,生成
,生成![]() 转移电子的物质的量为
转移电子的物质的量为![]() ;当生成NaCl和
;当生成NaCl和![]() 时,
时,![]() 消耗
消耗![]() ,生成
,生成![]() 转移电子的物质的量为
转移电子的物质的量为![]() ,所以如果反应中转移的电子为n mol,则
,所以如果反应中转移的电子为n mol,则![]() ,故A错误;
,故A错误;
B.令![]() ,
,![]() ,
,![]() ,生成NaCl获得的电子为
,生成NaCl获得的电子为![]() ,生成NaClO、
,生成NaClO、![]() 失去的电子为
失去的电子为![]() ,得失电子不相等,故B错误;
,得失电子不相等,故B错误;
C.若氯气和NaOH只发生反应![]() ,则消耗氯气为
,则消耗氯气为![]() ,若只发生反应
,若只发生反应![]() ,消耗的氯气为
,消耗的氯气为![]() ,所以与NaOH反应的氯气物质的量为
,所以与NaOH反应的氯气物质的量为![]() ,故C错误;
,故C错误;
D.当溶液中![]() :
:![]() :1时,则Cl原子失去的电子数为10,生成NaCl得到的电子数为1,所以NaCl的计量数为10,反应的离子方程式为:
:1时,则Cl原子失去的电子数为10,生成NaCl得到的电子数为1,所以NaCl的计量数为10,反应的离子方程式为:![]() ,故D正确;
,故D正确;
故答案选D。

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
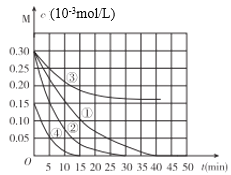
【题目】用Na2FeO4溶液氧化废水中的还原性污染物M,为研究降解效果.设计如下对比实验探究温度、浓度、pH、催化剂对降解速率和效果的影响,实验测得M的浓度与时间关系如图所示,下列说法不正确的是( )
实验编号 | 温度°C | pH |
① | 25 | 1 |
② | 45 | 1 |
③ | 25 | 7 |
④ | 25 | 1 |
A.实验①在15min内M的降解速率为1.33×10-5mol/(L·min)
B.若其他条件相同,实验①②说明升高温度,M降解速率增大
C.若其他条件相同,实验①③证明pH越高,越不利于M的降解
D.实验①④说明M的浓度越小,降解的速率越快