题目内容
【题目】氮氧化物是形成光化学烟雾和酸雨的重要原因。人们研究了诸多有关氮氧化物的性质,请回答下列问题:
(1)处理NOx的一种方法是利用甲烷催化还原NOx。
CH4(g)+4NO2(g)=4NO(g)+CO2(g)+2H2O(g) K1
CH4(g)+2NO2(g)=N2(g)+CO2(g)+2H2O(g) K2
CH4(g)+4NO(g)=2N2(g)+CO2(g)+2H2O(g) K3
K1、K2、K3依次为三个反应的平衡常数,则K3=__(用K1、K2表示)。
(2)在恒容密闭容器中通入等物质的量的CO和NO,在一定条件下发生反应:2CO(g)+2NO(g)![]() N2(g)+2CO2(g),测得NO的平衡转化率与温度及压强的关系如图所示:
N2(g)+2CO2(g),测得NO的平衡转化率与温度及压强的关系如图所示:
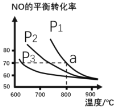
①对于气相反应,用某组分(B)的平衡分压强p(B)代替物质的量浓度c(B)也可表示平衡常数kp,如果p1=1.65MPa,求a点的平衡常数kp=__(MPa)1(结果保留3位有效数字,分压=总压×物质的量分数)。
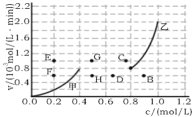
②为探究速率与浓度的关系,该实验中,根据相关实验数据,粗略绘制了2条速率—浓度关系曲线:v正~c(NO)和v逆~c(CO2)则:与曲线v正~c(NO)相对应的是图中曲线__(填“甲”或“乙”)。当降低反应体系的温度,反应一段时间后,重新达到平衡,v正和v逆相应的平衡点分别为___(填字母)。
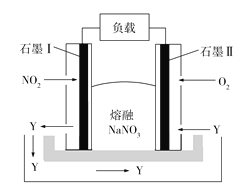
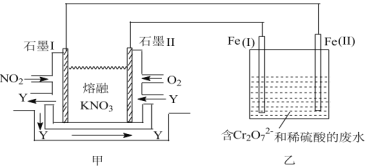
(3)利用电化学原理,将NO2、O2和熔融的KNO3制成燃料电池,模拟工业电解法来处理含Cr2O72的废水,如图所示;电解过程中溶液发生反应:Cr2O72+6Fe2++14H+=2Cr3++6Fe3++7H2O。甲电池工作时,Y是气体,可循环使用。则石墨I附近发生的电极反应式为___。
(4)已知H3PO4为三元酸,Ka1=7.0×103mol·L1,Ka2=6.2×108mol·L1,Ka3=4.5×1013mol·L1。则Na2HPO4水溶液呈__。
【答案】![]() 21.2 乙 D、H NO2+NO3--e-=N2O5 碱
21.2 乙 D、H NO2+NO3--e-=N2O5 碱
【解析】
(1)对已知热化学方程式编号,依据已知的热化学方程式利用盖斯定律构造CH4(g)+4NO(g)=2N2(g)+CO2(g)+2H2O(g),然后根据关系式得到平衡常数的关系;
(2)①对于气相反应,用某组分(B)的平衡压强p(B)代替物质的量浓度c(B)也可表示平衡常数(记作Kp),平衡常数等于生成物平衡分压幂次方乘积除以反应物平衡分压幂次方乘积得到,结合化学平衡三段式列式计算,设体积为1L,a点NO转化率为70%,据此计算;
②由三段式得的物质的物质的量分数,带入公式计算可得;
③NO是反应物,CO2是生成物,随反应进行,NO浓度减小,CO2浓度增大,降低反应体系的温度,v正~c(NO)和v逆~c(CO2)均减小,该反应为放热反应,平衡向正反应方向移动;
(3)由题给示意图可知,甲电池工作时,通入二氧化氮的一极为燃料电池的负极;
(4)根据Na2HPO4的电离常数和水解常数的相对大小判断Na2HPO4在水溶液的酸碱性。
(1)①CH4(g)+4NO2(g)=4NO(g)+CO2(g)+2H2O(g) K1
②CH4(g)+2NO2(g)=N2(g)+CO2(g)+2H2O(g) K2
③CH4(g)+4NO(g)=2N2 (g)+CO2(g)+2H2O(g) K3
由盖斯定律得到②![]() 2-①可得③,故对应的三个反应的平衡常数K1、K2、K3之间的关系为:K3=
2-①可得③,故对应的三个反应的平衡常数K1、K2、K3之间的关系为:K3=![]() ;
;
(2)①根据上述分析可知,
平衡气体总物质的量=0.3 mol +0.3 mol +0.35 mol +0.7 mol=1.65mol,因该反应的平衡常数的表达式Kp=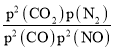 ,若P1=1.65MPa,用平衡分压代替平衡浓度计算,分压=总压×物质的量分数,则a点的平衡常数kp=
,若P1=1.65MPa,用平衡分压代替平衡浓度计算,分压=总压×物质的量分数,则a点的平衡常数kp=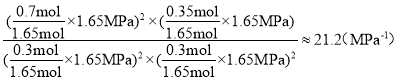 ,故答案为:21.2;
,故答案为:21.2;
③NO是反应物,CO2是生成物,随反应进行,NO浓度减小,CO2浓度增大,则由图可知,与曲线v正~c(NO)相对应的是图中曲线乙;降低反应体系的温度,v正~c(NO)和v逆~c(CO2)均减小,该反应为放热反应,平衡向正反应方向移动,c(NO)减小、c(CO2)增大,则v正和v逆相应的平衡点分别为D和H,故答案为:乙;D、H;
(3)由题给示意图可知,甲电池工作时,通入二氧化氮的一极为燃料电池的负极,二氧化氮在负极失电子发生氧化反应生成五氧化二氮,电极反应式为NO2+NO3--e-=N2O5;
(4)Na2HPO4在水溶液中发生水解反应,水解平衡为HPO42—+H2O![]() H2PO4—+OH—,水解平衡常数Kh2=
H2PO4—+OH—,水解平衡常数Kh2=![]() =
=![]() =
=![]() =1.6×10—7>Ka3=4.5×1013,HPO42-的水解程度大于电离程度,故溶液显碱性,故答案为:碱。
=1.6×10—7>Ka3=4.5×1013,HPO42-的水解程度大于电离程度,故溶液显碱性,故答案为:碱。

 教学练新同步练习系列答案
教学练新同步练习系列答案 课前课后同步练习系列答案
课前课后同步练习系列答案 课堂小作业系列答案
课堂小作业系列答案【题目】等质量的铁与过量的盐酸在不同的实验条件下进行反应,测定反应过程中产生氢气体积V,根据相关数据所绘制的图象如图所示,则曲线a、b、c、d所对应的实验组别可能依次是( )
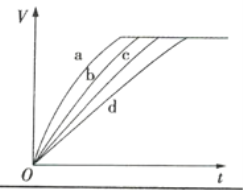
实验组别 | c(HCl)/(mol·L-1) | 温度/℃ | 形状(Fe) |
1 | 2.0 | 30 | 块状 |
2 | 2.5 | 30 | 块状 |
3 | 2.5 | 50 | 粉末状 |
4 | 2.5 | 30 | 粉末状 |
A.4、3、2、1B.1、2、3、4
C.3、4、2、1D.1、2、4、3
【题目】Ⅰ.氮的固定是几百年来科学家一直研究的课题。
(1)下表列举了不同温度下大气固氮和工业固氮的部分K值。
反应 | 大气固氮 N2(g)+O2(g) | 工业固氮 N2(g)+3H2(g) | |||
温度/℃ | 27 | 2000 | 25 | 400 | 450 |
K | 3.8×10﹣31 | 0.1 | 5×108 | 0.507 | 0.152 |
①分析数据可知:大气固氮反应属于_____(填“吸热”或“放热”)反应。
②分析数据可知;人类不适合大规模模拟大气固氮的原因__________________________。
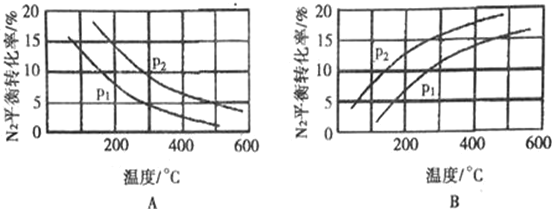
(2)工业固氮反应中,在其他条件相同时,分别测定N2的平衡转化率在不同压强(P1、P2)下随温度变化的曲线,如图所示的图示中,正确的是___(填“A”或“B”);比较P1、P2的大小关系:P1______P2(填“>”、“=” 或“<”)。
Ⅱ. 目前工业合成氨的原理是:N2(g)+3H2(g)![]() 2NH3(g)
2NH3(g)
(3)在一定温度下,将1mol N2和3mol H2混合置于体积不变的密闭容器中发生反应,达到平衡状态时,测得气体总物质的量为2.8mol。达平衡时,H2的转化率α1=____。