题目内容
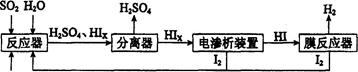
(14分)工业上用硫碘开路循环联产氢气和硫酸的工艺流程如下图所示:
回答下列问题:
(1)在反应器中发生反应的化学方程式是______________。
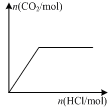
(2)在膜反应器中发生反应:2HI(g) H2(g)十I2 △H>0。若在一定条件下密闭容器中加入l mol HI(g), n(H2)随时间(t)的变化如图所示:
H2(g)十I2 △H>0。若在一定条件下密闭容器中加入l mol HI(g), n(H2)随时间(t)的变化如图所示:
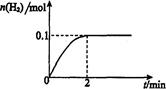
①该温度下,反应平衡常数K=_______,若升高温度,K值将_______
(填“增大”、“减小”或“不变?’)。
②用化学平衡原理解释使用膜反应器及时分离出H2的目的是___________________
(3)电渗析装置如下图所示:
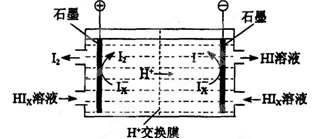
①结合电极反应式解释阴极区HIx转化为HI的原理是______________________________
②该装置中发生的总反应的化学方程式是________________________
(4)上述工艺流程中循环利用的物质是_________。

回答下列问题:
(1)在反应器中发生反应的化学方程式是______________。
(2)在膜反应器中发生反应:2HI(g)
 H2(g)十I2 △H>0。若在一定条件下密闭容器中加入l mol HI(g), n(H2)随时间(t)的变化如图所示:
H2(g)十I2 △H>0。若在一定条件下密闭容器中加入l mol HI(g), n(H2)随时间(t)的变化如图所示:
①该温度下,反应平衡常数K=_______,若升高温度,K值将_______
(填“增大”、“减小”或“不变?’)。
②用化学平衡原理解释使用膜反应器及时分离出H2的目的是___________________
(3)电渗析装置如下图所示:

①结合电极反应式解释阴极区HIx转化为HI的原理是______________________________
②该装置中发生的总反应的化学方程式是________________________
(4)上述工艺流程中循环利用的物质是_________。
(1)SO2+xI2+2H2O=H2SO4+2HIx;(2)①1/64,增大;②及时分离出H2,使平衡正向移动,提高HI的分解率;(3)①在阴极区发生反应:Ix-+(x-1)e-=xI-,且阳极区的H+通过交换膜进入阴极区,得以生成HI溶液;② 2HIx (x-1)I2+2HI;(4) I2
(x-1)I2+2HI;(4) I2
 (x-1)I2+2HI;(4) I2
(x-1)I2+2HI;(4) I2试题分析:(1)根据流程示意图可知:在反应器中发生反应的化学方程式是SO2+xI2+2H2O=H2SO4+2HIx;(2)①该温度下,反应平衡常数
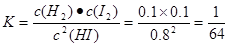 ;由于该反应的正反应是吸热反应,实验根据平衡移动原理,升高温度,化学平衡向吸热反应方向移动,实验化学平衡常数K值将增大;②使用膜反应器及时分离出H2,也就是减小了生成物的浓度,根据平衡移动原理,化学平衡向正反应方向移动,可以产生更多的生成物,从而提高了HI的分解率。(3)①由于阴极是与电源的负极连接的电极,有较多的负电荷,所以在阴极上发生反应:Ix-+(x-1)e-=xI-,根据同种电荷相互排斥,异种电荷相互吸引的原则,阳极区的H+通过交换膜进入阴极区,从而生成HI溶液;②根据电极反应式可知:该装置中发生的总反应的化学方程式是2HIx
;由于该反应的正反应是吸热反应,实验根据平衡移动原理,升高温度,化学平衡向吸热反应方向移动,实验化学平衡常数K值将增大;②使用膜反应器及时分离出H2,也就是减小了生成物的浓度,根据平衡移动原理,化学平衡向正反应方向移动,可以产生更多的生成物,从而提高了HI的分解率。(3)①由于阴极是与电源的负极连接的电极,有较多的负电荷,所以在阴极上发生反应:Ix-+(x-1)e-=xI-,根据同种电荷相互排斥,异种电荷相互吸引的原则,阳极区的H+通过交换膜进入阴极区,从而生成HI溶液;②根据电极反应式可知:该装置中发生的总反应的化学方程式是2HIx (x-1)I2+2HI;(4)在上述工艺流程中循环利用的物质是I2。
(x-1)I2+2HI;(4)在上述工艺流程中循环利用的物质是I2。
练习册系列答案
相关题目
 cZ(g)+dW(g)反应达到平衡后,将气体体积压缩到原来的一半,当再次达到平衡时,W的浓度为原平衡状态的1.8倍。下列叙述正确的是( )
cZ(g)+dW(g)反应达到平衡后,将气体体积压缩到原来的一半,当再次达到平衡时,W的浓度为原平衡状态的1.8倍。下列叙述正确的是( ) 
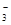
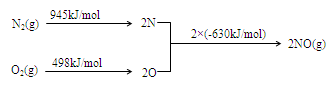
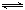 2NO(g)△H= 。
2NO(g)△H= 。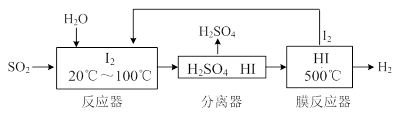
 NiO(OH)+MH,电池放电时,负极电极反应式为 ; 充电完成时,全部转化为NiO(OH),若继续充电,将在一个电极产生O2,O2扩散到另一个电极发生电极反应被消耗,从而避免产生的气体引起电池爆炸。
NiO(OH)+MH,电池放电时,负极电极反应式为 ; 充电完成时,全部转化为NiO(OH),若继续充电,将在一个电极产生O2,O2扩散到另一个电极发生电极反应被消耗,从而避免产生的气体引起电池爆炸。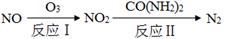
 SO3(g)+NO(g) △H=-41.8 kJ·mol-1
SO3(g)+NO(g) △H=-41.8 kJ·mol-1
 2(t-BuNO) 。该温度下该反应在CCl4溶剂中的平衡常数为1.4。
2(t-BuNO) 。该温度下该反应在CCl4溶剂中的平衡常数为1.4。 
 CO2(g)+H2(g) ΔH=Q,其平衡常数随温度变化如下表所示:
CO2(g)+H2(g) ΔH=Q,其平衡常数随温度变化如下表所示: