题目内容
(16分)NO和NO2是常见的氮氧化物,研究它们的综合利用有重要意义。
(1)氮氧化物产生的环境问题有 (填一种)。
(2)氧化—还原法消除氮氧化物的转化如下: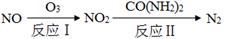
①反应Ⅰ为:NO+O3=NO2+O2,生成11.2 L O2(标准状况)时,转移电子的物质的量是 mol。
②反应Ⅱ中,当n(NO2)∶n[CO(NH2)2]=3∶2时,反应的化学方程式是 。
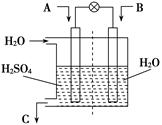
(3)硝化法是一种古老的生产硫酸的方法,同时实现了氮氧化物的循环转化,主要反应为:
NO2(g)+SO2(g) SO3(g)+NO(g) △H=-41.8 kJ·mol-1
SO3(g)+NO(g) △H=-41.8 kJ·mol-1
①已知:2SO2(g)+O2(g) 2SO3(g) △H=-196.6 kJ·mol-1
2SO3(g) △H=-196.6 kJ·mol-1
写出NO和O2反应生成NO2的热化学方程式 。
②一定温度下,向2 L恒容密闭容器中充入NO2和SO2各1 mol,5min达到平衡,此时容器中NO 和NO2的浓度之比为3∶1,则NO2的平衡转化率是 。
③上述反应达平衡后,其它条件不变时,再往容器中同时充入
NO2、SO2、SO3、NO各1mol,平衡 (填序号)。
A.向正反应方向移动
B.向逆反应方向移动
C.不移动
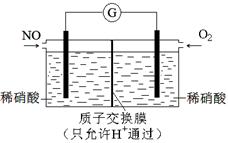
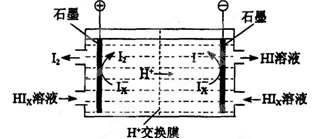
(4)某化学兴趣小组构想将NO转化为HNO3,装置如图,电极为多孔惰性材料。则负极的电极反应式是 。
(1)氮氧化物产生的环境问题有 (填一种)。
(2)氧化—还原法消除氮氧化物的转化如下:
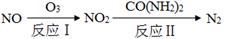
①反应Ⅰ为:NO+O3=NO2+O2,生成11.2 L O2(标准状况)时,转移电子的物质的量是 mol。
②反应Ⅱ中,当n(NO2)∶n[CO(NH2)2]=3∶2时,反应的化学方程式是 。
(3)硝化法是一种古老的生产硫酸的方法,同时实现了氮氧化物的循环转化,主要反应为:
NO2(g)+SO2(g)
 SO3(g)+NO(g) △H=-41.8 kJ·mol-1
SO3(g)+NO(g) △H=-41.8 kJ·mol-1①已知:2SO2(g)+O2(g)
 2SO3(g) △H=-196.6 kJ·mol-1
2SO3(g) △H=-196.6 kJ·mol-1写出NO和O2反应生成NO2的热化学方程式 。
②一定温度下,向2 L恒容密闭容器中充入NO2和SO2各1 mol,5min达到平衡,此时容器中NO 和NO2的浓度之比为3∶1,则NO2的平衡转化率是 。
③上述反应达平衡后,其它条件不变时,再往容器中同时充入
NO2、SO2、SO3、NO各1mol,平衡 (填序号)。
A.向正反应方向移动
B.向逆反应方向移动
C.不移动
(4)某化学兴趣小组构想将NO转化为HNO3,装置如图,电极为多孔惰性材料。则负极的电极反应式是 。

(1)产生光化学烟雾或形成酸雨(1分) (2)①1(2分)
②6NO2+4CO(NH2)2=7N2+8H2O+4CO2(3分)
(3)①2NO(g)+O2(g) = 2NO2(g) △H=-113.0 kJ·mol-1(3分) ②75%(2分)③A(2分)
(4)NO-3e-+2H2O=NO3-+4H+(3分)
②6NO2+4CO(NH2)2=7N2+8H2O+4CO2(3分)
(3)①2NO(g)+O2(g) = 2NO2(g) △H=-113.0 kJ·mol-1(3分) ②75%(2分)③A(2分)
(4)NO-3e-+2H2O=NO3-+4H+(3分)
试题分析:(1)氮氧化物产生的环境问题有产生光化学烟雾或形成酸雨等。
(2)①根据反应NO+O3=NO2+O2可知,每生成生成1mol氧气,反应中氮元素的化合价就从+2价升高到+4价,失去2个电子,则11.2 L O2(标准状况)即0.5mol氧气时,转移电子的物质的量是1mol。
②反应ⅡNO2中氮元素的化合价是+4价,而尿素中氮元素的化合价是-3价,当n(NO2)∶n[CO(NH2)2]=3∶2时,根据电子得失守恒可知,氮原子均转化为氮气,则根据原子守恒可知,其余产物是水和CO2,所以反应的化学方程式是6NO2+4CO(NH2)2=7N2+8H2O+4CO2。
(3)①已知:反应2SO2(g)+O2(g)
 2SO3(g) △H=-196.6 kJ·mol-1、NO2(g)+SO2(g)
2SO3(g) △H=-196.6 kJ·mol-1、NO2(g)+SO2(g) SO3(g)+NO(g) △H=-41.8 kJ·mol-1,则根据盖斯定律可知前者减去后者乘以2即得到2NO(g)+O2(g) = 2NO2(g),则△H=-196.6 kJ·mol-1+41.8 kJ·mol-1×2=-113.0 kJ·mol-1。
SO3(g)+NO(g) △H=-41.8 kJ·mol-1,则根据盖斯定律可知前者减去后者乘以2即得到2NO(g)+O2(g) = 2NO2(g),则△H=-196.6 kJ·mol-1+41.8 kJ·mol-1×2=-113.0 kJ·mol-1。② NO2(g)+SO2(g)
 SO3(g)+NO(g)
SO3(g)+NO(g)起始量(mol) 1 1 0 0
转化量(mol) x x x x
平衡量(mol)1-x 1-x x x
则根据容器中NO 和NO2的浓度之比为3∶1可知x:(1-x)=3∶1
解得x=0.75
所以NO2的平衡转化率是75%
③反应前后体积不变,则可以用物质的量代替浓度计算平衡常数,则根据②可知,该温度下反应的平衡常数K=
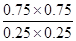 =9。若其它条件不变时,再往容器中同时充入NO2、SO2、SO3、NO各1mol,则此时
=9。若其它条件不变时,再往容器中同时充入NO2、SO2、SO3、NO各1mol,则此时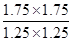 =1.96<9,所以反应向正反应方向进行,答案选A。
=1.96<9,所以反应向正反应方向进行,答案选A。(4)原电池中负极失去电子,发生氧化反应,因此NO在负极通入,氧气在正极通入。电解质溶液显酸性,因此负极电极反应式为NO-3e-+2H2O=NO3-+4H+。

练习册系列答案
相关题目

 4NO+6H2O(g),下列叙述不正确的是 ( )
4NO+6H2O(g),下列叙述不正确的是 ( )  2SO3(g)在一个体积不变的密闭容器中反应,达到平衡状态的标志是( )
2SO3(g)在一个体积不变的密闭容器中反应,达到平衡状态的标志是( )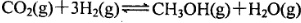 ,5 min后反应达到平衡时c(CH3OH)为0.2 mol
,5 min后反应达到平衡时c(CH3OH)为0.2 mol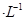 。CO2(g)的平衡物质的量浓度c(CO2)与温度关系如图所示。下列说法错误的是
。CO2(g)的平衡物质的量浓度c(CO2)与温度关系如图所示。下列说法错误的是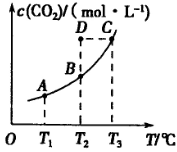
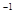
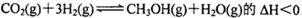
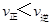
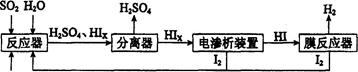
 H2(g)十I2 △H>0。若在一定条件下密闭容器中加入l mol HI(g), n(H2)随时间(t)的变化如图所示:
H2(g)十I2 △H>0。若在一定条件下密闭容器中加入l mol HI(g), n(H2)随时间(t)的变化如图所示: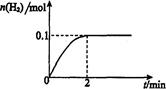
 I3-(aq)。在反应的平衡体系中,c(I3-)与温度T的关系如图所示(曲线上的任何一点都表示平衡状态)。
I3-(aq)。在反应的平衡体系中,c(I3-)与温度T的关系如图所示(曲线上的任何一点都表示平衡状态)。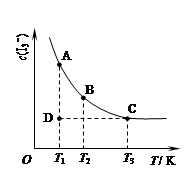
 2C,达到化学反应限度时,B的物质的量可能是( )
2C,达到化学反应限度时,B的物质的量可能是( )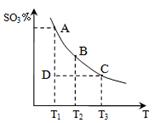
 2SO3(g)的△H____0(填“>”或“<”),若在恒温、恒压条件下向上述平衡体系中通入氦气,平衡 移动(填“向左”、“向右”或“不移动”);
2SO3(g)的△H____0(填“>”或“<”),若在恒温、恒压条件下向上述平衡体系中通入氦气,平衡 移动(填“向左”、“向右”或“不移动”); 2CO2+N2。它的优点是 ;
2CO2+N2。它的优点是 ;