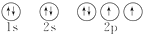题目内容
5.在原子结构示意图中,M层最多能容纳电子数目为( )| A. | 2 | B. | 8 | C. | 18 | D. | 32 |
分析 根据每层最多容纳2n2个电子计算.
解答 解:根据核外电子排布规律可知,每层最多容纳2n2个电子,M层为第三层,则M层最多能容纳电子数目为2×32=18;
故选C.
点评 本题考查了原子核外电子排布规律,题目难度不大,注意每层最多容纳2n2个电子.

练习册系列答案
相关题目
14.下列说法中正确的是( )
| A. | SO2、SiO2、CO均为酸性氧化物 | |
| B. | 水泥、陶瓷、硅酸和水晶均为硅酸盐产品 | |
| C. | 烧碱、冰醋酸、四氯化碳均为电解质 | |
| D. | 漂白粉、水玻璃、氨水和汽油均为混合物 |
15.下列说法正确的是( )
| A. | 摩尔是国际单位制规定的基本物理量 | |
| B. | 阿伏伽德罗常数被规定为12g 12C中所含的碳原子数 | |
| C. | 我们可以利用物质的量描述常见物质,如1mol 铅笔… | |
| D. | 物质的摩尔质量等于该物质的相对分子质量 |
 PM2.5污染跟工业燃煤密切相关,燃煤还同时排放大量的SO2和NOX.
PM2.5污染跟工业燃煤密切相关,燃煤还同时排放大量的SO2和NOX.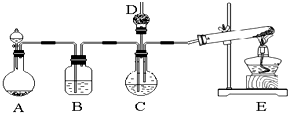
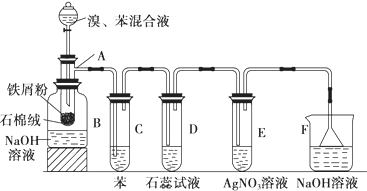
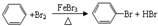 ,该有机反应的类型为取代反应.
,该有机反应的类型为取代反应.