题目内容
14.下列说法中正确的是( )| A. | SO2、SiO2、CO均为酸性氧化物 | |
| B. | 水泥、陶瓷、硅酸和水晶均为硅酸盐产品 | |
| C. | 烧碱、冰醋酸、四氯化碳均为电解质 | |
| D. | 漂白粉、水玻璃、氨水和汽油均为混合物 |
分析 A、和碱反应生成盐和水的氧化物为酸性氧化物;
B、水晶是二氧化硅晶体,硅酸是酸不是盐;
C、水溶液中或熔融状态下导电的化合物为电解质;
D、不同物质组成的为混合物,同一种物质组成的为纯净物;
解答 解:A、和碱反应生成盐和水的氧化物为酸性氧化物,SO2、SiO2、属于酸性氧化物,CO不能和碱反应生成盐,属于不成盐氧化物,故A错误;
B、水晶是二氧化硅晶体,不是硅酸盐产品,水泥、陶瓷均为硅酸盐产品,硅酸和水晶不是硅酸盐产品,故B错误;
C、水溶液中或熔融状态下导电的化合物为电解质,烧碱、冰醋酸水溶液中电离出离子能导电,属于电解质,四氯化碳为非电解质,故C错误;
D、不同物质组成的为混合物,同一种物质组成的为纯净物,漂白粉、水玻璃、氨水和汽油都是由不同物质组成的均为混合物,故D正确;
故选D.
点评 不同考查了物质组成和分类的分析,主要是物质组成、名称的掌握,注意知识积累,题目较简单.

练习册系列答案
相关题目
5.在原子结构示意图中,M层最多能容纳电子数目为( )
| A. | 2 | B. | 8 | C. | 18 | D. | 32 |
19.分类是学习和研究化学的一种重要思想方法,下列关于物质分类的说法中正确的是( )
| A. | 漂白粉、胆矾都是混合物 | |
| B. | 烧碱、纯碱都是离子化合物 | |
| C. | 二氧化碳、二氧化氮都是酸性氧化物 | |
| D. | 水、氨水都是弱电解质 |
6.铁屑溶于过量稀硫酸,过滤后向滤液中加入过量氨水,有白色沉淀生成,过滤,在空气中加热沉淀至质量不再发生变化为止,得到红棕色残渣,上述沉淀和残渣分别是( )
| A. | Fe(OH)3 Fe2O3 | B. | Fe(OH)2 Fe2O3 | C. | Fe(OH)2 Fe(OH)3 | D. | Fe(OH)2 Fe3O4 |
3.有Al、CuO、Fe2O3组成的混合物共10.0g,放入200mL某浓度的硫酸溶液中,混合物完全溶解,当再加入280mL 1.0mol•L-1的NaOH溶液时,得到的沉淀最多.上述硫酸溶液的浓度为( )
| A. | 1.4 mol•L-1 | B. | 1.0 mol•L-1 | C. | 0.7 mol•L-1 | D. | 0.5mol•L-1 |

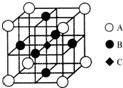 信息一:铬同镍、钴、铁等金属可以构成高温合金、电热合金、精密合金等,用于航空、宇航、电器及仪表等工业部门.
信息一:铬同镍、钴、铁等金属可以构成高温合金、电热合金、精密合金等,用于航空、宇航、电器及仪表等工业部门.