题目内容
17.下列轨道表示式所示的氧原子的核外电子排布中,氧原子处于基态的是( )| A. | 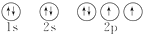 | B. |  | C. |  | D. |  |
分析 根据原子核外电子排布原则:电子优先单独占据1个轨道,且自旋方向相同是,能量最低,根据分析.
解答 解:原子核外电子排布原则:能级相同的轨道中电子优先单独占据1个轨道,且自旋方向相同,原子的能量最低,O原子能量最低排布,即氧原子处于基态的是: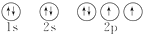 ;
;
故选A.
点评 本题考查核外电子排布规律,难度不大,注意核外电子排布规律的理解与灵活运用.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
8. 二氧化碳是引起“温室效应”的主要物质,节能减排,高效利用能源,能够减少二氧化碳的排放.
二氧化碳是引起“温室效应”的主要物质,节能减排,高效利用能源,能够减少二氧化碳的排放.
(1)汽车尾气的主要污染物是NO以及燃料燃烧不完全所产生的CO,它们是现代化城市的重要大气污染物,为了减轻汽车尾气造成的大气污染,人们开始探索利用NO和CO在一定条件下转化为两种无毒气体E和F的方法(已知该反应△H<0).在2L密闭容器中加入一定量NO和CO,当温度分别在T1和T2时,测得各物质平衡时物质的量如下表:
①请结合上表数据,写出NO与CO反应的化学方程式2CO+2NO?2CO2+N2.
②上述反应T1℃时的平衡常数为K1,T2℃时的平衡常数为K2,根据表中数据计算K1=3200.根据表中数据判断,温度T1和T2的关系是(填序号)A.
A.T1>T2 B.T1<T2 C.T1=T2 D.无法比较
(2)在一个体积为1L的真空容器中,加入0.5mol CaCO3,T℃时,发生反应:CaCO3(s)?CaO(s)+CO2(g),测得c(CO2)=0.2mol/L.温度不变,压缩容积为0.5L,则c(CO2)的变化范围为:0.2mol/L≤c(CO2)<0.4mol/L.
(3)已知CH4、H2和CO的燃烧热分别为890.3kJ/mol,285.8kJ/mol和283.0kJ/mol,工业上利用天然气(主要成分是CH4)与CO2进行高温重整制备CO和H2,写出该反应的热化学方程式:CH4(g)+CO2(g)=2CO(g)+2H2(g)△H=+247.3 kJ•mol -1.
(4)氨硼烷(H3BNH3)一种具有潜在应用前景的氢存储介质,吸收H2后的氨硼烷作电池负极材料(用MH表示),利用其产生的电能进行硫酸铜溶液的电解实验,如图所示.
①电池放电时,负极的电极反应式为MH+OH--e-═M+H2O
②若电流表的指针指向500mA,假设电流强度不变,当电解池中的Cu2+完全析出,理论上需要时间3.86×104s( 法拉第常数F=9.65×104C•mol-1)
 二氧化碳是引起“温室效应”的主要物质,节能减排,高效利用能源,能够减少二氧化碳的排放.
二氧化碳是引起“温室效应”的主要物质,节能减排,高效利用能源,能够减少二氧化碳的排放.(1)汽车尾气的主要污染物是NO以及燃料燃烧不完全所产生的CO,它们是现代化城市的重要大气污染物,为了减轻汽车尾气造成的大气污染,人们开始探索利用NO和CO在一定条件下转化为两种无毒气体E和F的方法(已知该反应△H<0).在2L密闭容器中加入一定量NO和CO,当温度分别在T1和T2时,测得各物质平衡时物质的量如下表:
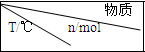 | NO | CO | E | F |
| 初始 | 0.100 | 0.100 | 0 | 0 |
| T1 | 0.020 | 0.020 | 0.080 | 0.040 |
| T2 | 0.010 | 0.010 | 0.090 | 0.045 |
②上述反应T1℃时的平衡常数为K1,T2℃时的平衡常数为K2,根据表中数据计算K1=3200.根据表中数据判断,温度T1和T2的关系是(填序号)A.
A.T1>T2 B.T1<T2 C.T1=T2 D.无法比较
(2)在一个体积为1L的真空容器中,加入0.5mol CaCO3,T℃时,发生反应:CaCO3(s)?CaO(s)+CO2(g),测得c(CO2)=0.2mol/L.温度不变,压缩容积为0.5L,则c(CO2)的变化范围为:0.2mol/L≤c(CO2)<0.4mol/L.
(3)已知CH4、H2和CO的燃烧热分别为890.3kJ/mol,285.8kJ/mol和283.0kJ/mol,工业上利用天然气(主要成分是CH4)与CO2进行高温重整制备CO和H2,写出该反应的热化学方程式:CH4(g)+CO2(g)=2CO(g)+2H2(g)△H=+247.3 kJ•mol -1.
(4)氨硼烷(H3BNH3)一种具有潜在应用前景的氢存储介质,吸收H2后的氨硼烷作电池负极材料(用MH表示),利用其产生的电能进行硫酸铜溶液的电解实验,如图所示.
①电池放电时,负极的电极反应式为MH+OH--e-═M+H2O
②若电流表的指针指向500mA,假设电流强度不变,当电解池中的Cu2+完全析出,理论上需要时间3.86×104s( 法拉第常数F=9.65×104C•mol-1)
5.在原子结构示意图中,M层最多能容纳电子数目为( )
| A. | 2 | B. | 8 | C. | 18 | D. | 32 |
12.有关核外电子运动规律的描述错误的是( )
| A. | 核外电子质量很小,在原子核外绕核作高速运动 | |
| B. | 核外电子的运动规律与普通物体不同,不能用牛顿运动定律来解释 | |
| C. | 在电子云示意图中,通常用小黑点来表示电子绕核作高速圆周运动 | |
| D. | 在电子云示意图中,小黑点越密表示电子在核外空间单位体积内电子出现的概率越大 |
6.铁屑溶于过量稀硫酸,过滤后向滤液中加入过量氨水,有白色沉淀生成,过滤,在空气中加热沉淀至质量不再发生变化为止,得到红棕色残渣,上述沉淀和残渣分别是( )
| A. | Fe(OH)3 Fe2O3 | B. | Fe(OH)2 Fe2O3 | C. | Fe(OH)2 Fe(OH)3 | D. | Fe(OH)2 Fe3O4 |
7.下列有关电化学的图示完全正确的是( )
| A. | 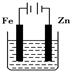 海水防止铁被腐蚀 | |
| B. | 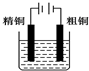 CuSO4精铜的精炼 | |
| C. |  ZnCl2溶液铁片镀锌 | |
| D. |  饱和食盐水验证NaCl溶液(含酚酞)电解产物 |

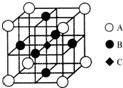 信息一:铬同镍、钴、铁等金属可以构成高温合金、电热合金、精密合金等,用于航空、宇航、电器及仪表等工业部门.
信息一:铬同镍、钴、铁等金属可以构成高温合金、电热合金、精密合金等,用于航空、宇航、电器及仪表等工业部门.