��Ŀ����
����Ŀ��I��ͨ��״���£�X��Y��Z��������̬���ʣ�X�����Ԫ���ǵ�������ԭ�Ӱ뾶��С��Ԫ�أ�ϡ������Ԫ�س��⣩��Y��Z����Ԫ��R��ɣ�Y��Ҫ�ֲ���ƽ��������У��ǵ���ı���ɡ��
��1��Y��Z�Ĺ�ϵ�ǣ�ѡ����ĸ��__________��
a��ͬλ�� b��ͬϵ�� c��ͬ�������� d��ͬ���칹��
��2����Y�Ͷ�������ֱ�ͨ��Ʒ����Һ������ʹƷ����ɫ����������ɫ����Һ������ߵ�ʵ�鷽��___________��
��3��ʵ�����Ʊ�X�Ļ�ѧ����ʽ_____________________________��
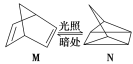
II�����ԭ���ڻ�ѧ��ҵ���й㷺Ӧ�á���ͼ��ʾһ�����أ�װ�е��Һa��X��Y������缫�壬ͨ��������ֱ����Դ��������ش��������⣺

��4����X��Y���Ƕ��Ե缫��a�DZ���NaCl��Һ��ʵ�鿪ʼʱ��ͬʱ�����߸����뼸�η�̪��Һ����
�ٵ�����X���ϵĵ缫��ӦʽΪ_____________����X�������۲쵽��������_________��
�ڣٵ缫�ϵĵ缫��ӦʽΪ_________________������õ缫��Ӧ����ķ�����___________��
��5����Ҫ�õ�ⷽ��������ͭ�����Һaѡ��CuSO4��Һ����
��X�缫�IJ�����__________���缫��ӦʽΪ________________________________��
��Y�缫�IJ�����__________���缫��ӦʽΪ________________________________����˵�������ʷ����ĵ缫��Ӧ����д����
���𰸡� c ������ɫ�����Һ������Һ�ָ���ɫ����ԭͨ������ΪSO2������Һ����죬��ԭͨ��������O3 MnO2+4HCl(Ũ) ![]() MnCl2+Cl2��+2H2O 2H++2e��==H2�� �ų����壬��Һ��� 2Cl����2e��==Cl2�� ��ʪ��ĵ⻯�ص�����ֽ����Y�缫��������ֽ����ɫ ��ͭ Cu2++2e��==Cu ��ͭ Cu��2e��==Cu2+
MnCl2+Cl2��+2H2O 2H++2e��==H2�� �ų����壬��Һ��� 2Cl����2e��==Cl2�� ��ʪ��ĵ⻯�ص�����ֽ����Y�缫��������ֽ����ɫ ��ͭ Cu2++2e��==Cu ��ͭ Cu��2e��==Cu2+
��������I��ͨ��״���£�X��Y��Z��������̬���ʣ�X�����Ԫ���ǵ�������ԭ�Ӱ뾶��С��Ԫ�أ�ϡ������Ԫ�س��⣩��X��Cl��Y��Z����Ԫ��R��ɣ�Y��Ҫ�ֲ���ƽ��������У��ǵ���ı���ɡ�����Y�dz�������Z��������R����Ԫ�ء�
��1�������ͳ���������Ԫ���γɵĵ��ʣ�����Ϊͬ�������壬��ѡc����2���������������ԣ�ʹƷ����Һ��ɫ����ɫ�Dz�����ġ�SO2ʹƷ����Һ��ɫ�ǿ���ģ���������ߵ�ʵ�鷽���Ǽ�����ɫ�����Һ������Һ�ָ���ɫ����ԭͨ������ΪSO2������Һ����죬��ԭͨ��������O3����3��ʵ�����Ʊ������Ļ�ѧ����ʽΪMnO2+4HCl(Ũ)![]() MnCl2+Cl2��+2H2O��
MnCl2+Cl2��+2H2O��
II����4����X�缫���Դ�ĸ�������������������Һ�е������ӷŵ磬��˵�����X���ϵĵ缫��ӦʽΪ2H++2e��==H2���������ӷŵ��ƻ���ˮ�ĵ���ƽ�⣬X�缫������������Ũ�ȴ��������ӣ���Һ�Լ��ԣ�������X�������۲쵽�������Ƿų����壬��Һ��졣�ڣٵ缫����������Һ�е������ӷŵ磬�缫��ӦʽΪ2Cl����2e��==Cl2������������ǿ�����ԣ�����õ缫��Ӧ����ķ����ǰ�ʪ��ĵ⻯�ص�����ֽ����Y�缫��������ֽ����ɫ����5���ٴ�ͭ����ʱ��ͭ����������ͭ�����������Դ����������������X�缫�IJ����Ǵ�ͭ���缫��ӦʽΪCu2++2e��==Cu����Y�缫�IJ����Ǵ�ͭ���缫��ӦʽΪCu��2e��==Cu2+��

 �Ķ��쳵ϵ�д�
�Ķ��쳵ϵ�д�