题目内容
如图1是硫酸的试剂标签上的部分内容.某次学生实验需要0.5mol?L-1H2SO4溶液480mL,若由你来配制所需溶液,请根据实验室已有的仪器和药品情况回答下列问题:
(1)容量瓶应如何检漏:______.
(2)实验中除量筒、烧杯外还需要的其他仪器______.
(3)计算所需浓硫酸的体积约为______mL;若将该硫酸与等体积的水混合,所得溶液中溶质的质量分数______49%(填“<”、“=”或“>”).
(4)配制过程中需先在烧杯中将浓硫酸进行稀释.稀释的操作方法是______.
(5)下列操作会引起所配溶液浓度偏大的是______(填字母).A.用量筒量取浓硫酸时,仰视量筒的刻度B.向容量瓶中转移时,有少量液体溅出C.定容时仰视刻度线D.定容后倒置摇匀后再正立时,发现液面低于刻度线
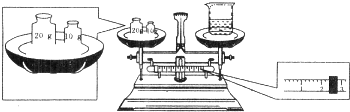
(6)温度计、量筒、滴定管的一部分如图2所示,下述读数(虚线所指刻度)及说法正确的是______(填字母).A.①是量筒,读数为2.5mLB.②是量筒,读数为2.5mLC.③是滴定管,读数为2.5mLD.①是温度计,读数为2.5℃

(1)容量瓶应如何检漏:______.
(2)实验中除量筒、烧杯外还需要的其他仪器______.
(3)计算所需浓硫酸的体积约为______mL;若将该硫酸与等体积的水混合,所得溶液中溶质的质量分数______49%(填“<”、“=”或“>”).
(4)配制过程中需先在烧杯中将浓硫酸进行稀释.稀释的操作方法是______.
(5)下列操作会引起所配溶液浓度偏大的是______(填字母).A.用量筒量取浓硫酸时,仰视量筒的刻度B.向容量瓶中转移时,有少量液体溅出C.定容时仰视刻度线D.定容后倒置摇匀后再正立时,发现液面低于刻度线
(6)温度计、量筒、滴定管的一部分如图2所示,下述读数(虚线所指刻度)及说法正确的是______(填字母).A.①是量筒,读数为2.5mLB.②是量筒,读数为2.5mLC.③是滴定管,读数为2.5mLD.①是温度计,读数为2.5℃

(1)容量瓶检漏的方法是加适量水后塞紧瓶塞倒置不漏水,然后正放,应注意瓶塞要旋转180度,再倒置看是否漏水,
故答案为:将瓶塞打开,加入少量水,塞好瓶塞,倒转不漏水,然后正放,把瓶塞旋转180度,再倒转不漏水,则说明该容量瓶不漏水;
(2)由于没有480mL的容量瓶,故应使用500mL的容量瓶,根据配制过程可知,还缺少500mL容量瓶、玻璃棒、胶头滴管,
故答案为:500mL容量瓶、玻璃棒、胶头滴管;
(3)由所给浓硫酸标签上的数据易求得该硫酸浓度为:18.4mol?L-1,故配制500mL0.5mol?L-1的稀溶液时约需要13.6mL浓硫酸,
故答案为:13.6;>;
(4)稀释浓硫酸时应将浓硫酸沿器壁慢慢加入到水中,并不断搅拌,操作方法为:向烧杯中先加入适量蒸馏水,再将量取的浓硫酸沿烧杯内壁慢慢倒入烧杯中,并用玻璃棒不断搅拌,
故答案为:向烧杯中先加入适量蒸馏水,再将量取的浓硫酸沿烧杯内壁慢慢倒入烧杯中,并用玻璃棒不断搅拌;
(5)仰视量筒时,量筒中实际液面高于看到的液面,导致硫酸取多了,结果偏高;B、C两个选项操作均引起结果偏低,
故答案为:A;
(6)A.量筒上没有0刻度值,故A错误;
B.量筒的读数能够读到0.1mL,图②中液体体积为2.5mL,故B正确;
C.滴定管读数时应保留两位小数,正确读数为2.50mL,故C错误;
D.只有温度计的0刻度下还有数据,且图示温度为2.5℃,故D正确;
故答案为:BD.
故答案为:将瓶塞打开,加入少量水,塞好瓶塞,倒转不漏水,然后正放,把瓶塞旋转180度,再倒转不漏水,则说明该容量瓶不漏水;
(2)由于没有480mL的容量瓶,故应使用500mL的容量瓶,根据配制过程可知,还缺少500mL容量瓶、玻璃棒、胶头滴管,
故答案为:500mL容量瓶、玻璃棒、胶头滴管;
(3)由所给浓硫酸标签上的数据易求得该硫酸浓度为:18.4mol?L-1,故配制500mL0.5mol?L-1的稀溶液时约需要13.6mL浓硫酸,
故答案为:13.6;>;
(4)稀释浓硫酸时应将浓硫酸沿器壁慢慢加入到水中,并不断搅拌,操作方法为:向烧杯中先加入适量蒸馏水,再将量取的浓硫酸沿烧杯内壁慢慢倒入烧杯中,并用玻璃棒不断搅拌,
故答案为:向烧杯中先加入适量蒸馏水,再将量取的浓硫酸沿烧杯内壁慢慢倒入烧杯中,并用玻璃棒不断搅拌;
(5)仰视量筒时,量筒中实际液面高于看到的液面,导致硫酸取多了,结果偏高;B、C两个选项操作均引起结果偏低,
故答案为:A;
(6)A.量筒上没有0刻度值,故A错误;
B.量筒的读数能够读到0.1mL,图②中液体体积为2.5mL,故B正确;
C.滴定管读数时应保留两位小数,正确读数为2.50mL,故C错误;
D.只有温度计的0刻度下还有数据,且图示温度为2.5℃,故D正确;
故答案为:BD.

练习册系列答案
 假期作业暑假成长乐园新疆青少年出版社系列答案
假期作业暑假成长乐园新疆青少年出版社系列答案
相关题目