题目内容
(12分)脱硫技术能有效控制SO2对空气的污染。
(1)向煤中加入石灰石可减少燃烧产物中SO2的含量,该反应的化学方程式是_______。
(2)海水呈弱碱性,主要含有Na+、K+、Ca2+、Mg2+、Cl-、SO42-、Br-、HCO3-等离子。含SO2的烟气可利用海水脱硫,其工艺流程如下图所示:
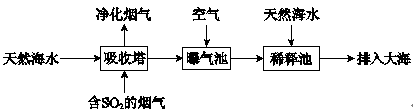
①向曝气池中通入空气的目的是_______。
②通入空气后曝气池中海水与天然海水相比,浓度有明显不同的离子是_______。
a.Cl- b.SO42- c.Br- d.HCO3-
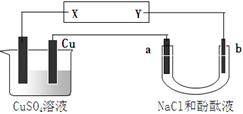
(3)用NaOH溶液吸收烟气中的SO2,将所得的Na2SO3溶液进行电解,可循环再生NaOH,同时得到H2SO4,其原理如下图所示。(电极材料为石墨)
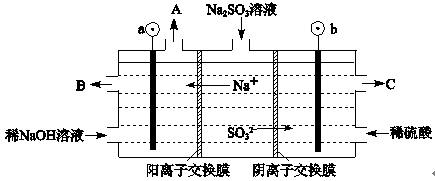
①图中a极要连接电源的(填“正”或“负”)_______极,C口流出的物质是_______。
②SO32-放电的电极反应式为_______。
③电解过程中阴极区碱性明显增强,用平衡移动原理解释原因_______。
(1)向煤中加入石灰石可减少燃烧产物中SO2的含量,该反应的化学方程式是_______。
(2)海水呈弱碱性,主要含有Na+、K+、Ca2+、Mg2+、Cl-、SO42-、Br-、HCO3-等离子。含SO2的烟气可利用海水脱硫,其工艺流程如下图所示:

①向曝气池中通入空气的目的是_______。
②通入空气后曝气池中海水与天然海水相比,浓度有明显不同的离子是_______。
a.Cl- b.SO42- c.Br- d.HCO3-
(3)用NaOH溶液吸收烟气中的SO2,将所得的Na2SO3溶液进行电解,可循环再生NaOH,同时得到H2SO4,其原理如下图所示。(电极材料为石墨)

①图中a极要连接电源的(填“正”或“负”)_______极,C口流出的物质是_______。
②SO32-放电的电极反应式为_______。
③电解过程中阴极区碱性明显增强,用平衡移动原理解释原因_______。
(1)2SO2 +O2 +2CaCO3=2CaSO4+2CO2
(2)①将H2SO3、HSO3-等氧化为SO42- ②bd
(3)①负 硫酸
② SO32-–2e-+H2O=SO42-+2H+
③H2O H++OH—,在阴极H+放电生成H2,c(H+)减小,水的电离平衡正向移动,碱性增强
H++OH—,在阴极H+放电生成H2,c(H+)减小,水的电离平衡正向移动,碱性增强
(2)①将H2SO3、HSO3-等氧化为SO42- ②bd
(3)①负 硫酸
② SO32-–2e-+H2O=SO42-+2H+
③H2O
 H++OH—,在阴极H+放电生成H2,c(H+)减小,水的电离平衡正向移动,碱性增强
H++OH—,在阴极H+放电生成H2,c(H+)减小,水的电离平衡正向移动,碱性增强试题分析:(1)向煤中加入石灰石起固硫的作用,该反应的化学方程式是2SO2 +O2 +2CaCO3=2CaSO4+2CO2 (2)含SO2的烟气可利用海水脱硫,向曝气池中通入空气的目的是把H2SO3、HSO3-等氧化为SO42-; 由上一问可知硫酸根浓度肯定增大,天然海水呈弱碱性,通入空气后曝气池中的海水会生成酸性物质会消耗HCO3- ,HCO3-会减少,所以通入空气后曝气池中海水与天然海水相比,浓度有明显不同的离子是 b.SO42- d.HCO3-
(3)根据电解池中阴阳离子的移动方向:阳离子移向阴极可以判断①图中a极要连接电源的负极,SO32-在阳极失去电子变成SO42-,所以C口流出的物质是H2SO4 ,SO32-放电的电极反应式为SO32-–2e-+H2O=SO42-+2H+ ,在阴极H+放电生成H2,c(H+)减小,水的电离平衡H2O
 H++OH—正向移动,所以碱性增强。
H++OH—正向移动,所以碱性增强。点评:原电池,电解池,电镀池等知识是常考的题目,其知识点比较单一,只要注意区分。原电池和电解池异同点:
(1)、电解名称不一样:原电池叫负极和正极,电解池叫阴极和阳极;
(2)、发生反应情况:都发生氧化还原反应,原电池为自发的,电解池是强迫的;
(3)、原电池是电源,电解池需要电源;
(4)、都有闭合回路;
(5)、负极和阳极发生氧化反应,失去电子,正极和阴极发生还原反应得到电子;
(6)、原电池是化学能转化为电能,而电解池是电能转化为化学能;
(7)、电解质中离子的移动方向:原电池中,阳离子往正极移动,阴离子往负极移动,在电解池中,阳离子往阴极移动,阴离子往阳极移动;
(8)、外电路中都靠自由电子导电,内电路中都靠离子导电;
(9)、本质都是氧化还原反应。
(10)、原电池的正极跟电解池的阳极相连,原电池的负极跟电解池的阴极相连。
只要学生学习过程中牢记并理解这些原电池和电解池异同点,便不难解答此题。

练习册系列答案
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案
相关题目
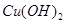 ,恰好恢复到电解前的pH和浓度,则电解过程中转移的电子的物质的量为:
,恰好恢复到电解前的pH和浓度,则电解过程中转移的电子的物质的量为:
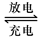 4LiCl +S+SO2,则下列叙述中不正确的是
4LiCl +S+SO2,则下列叙述中不正确的是