题目内容
7.100mL 1mol•L-1Al2(SO4)3溶液中,含Al3+0.2mol,含SO42-0.3mol,100mL5mol•L-1的蔗糖溶液中,所含蔗糖分子数与溶液中阴阳离子总数相同.分析 硫酸铝为强电解质,在水中完全电离,电离方程式:Al2 (SO4)3═2Al3++3SO42-,依据n=CV计算硫酸铝的物质的量,结合电离方程式计算铝离子、硫酸根离子的物质的量,再计算阴阳离子总数,依据C=$\frac{n}{V}$计算蔗糖的物质的量浓度.
解答 解:100mL 1mol•L-1Al2(SO4)3溶液中,含硫酸的铝的物质的量为:1mol•L-1×0.1L=0.1mol,硫酸铝为强电解质,在水中完全电离,电离方程式:Al2 (SO4)3═2Al3++3SO42-,
则:Al2 (SO4)3═2Al3++3SO42-,
1 2 3
0.1mol n(Al3+) n(SO42-)
所以:n(Al3+)=0.2mol;
n(SO42-)=0.3mol;
溶液中阴阳离子总数:0.2+0.3=0.5mol,
蔗糖的物质的量浓度C=$\frac{n}{V}$=$\frac{0.5mol}{0.1L}$=5mol/L;
故答案为:0.2;0.3;5.
点评 本题考查了电解质的电离及有关物质的量浓度计算,明确电解质强弱、物质的量浓度概念是解题关键,题目难度不大.

练习册系列答案
相关题目
17.已知浓H2SO4和Fe3+都可以将Cu氧化成Cu2+,浓H2SO4也可以将Br-氧化成Br2,Fe与Br2反应生成FeBr3.由此可以确定上述有关物质氧化性由强到弱的顺序为( )
| A. | 浓H2SO4 Br2 Fe3+ Cu2+ | B. | 浓H2SO4 Cu2+Fe3+ Br2 | ||
| C. | Br2 浓H2SO4 Fe3+Cu2+ | D. | Fe3+ Cu2+ Br2 浓H2SO4 |
18.下列说法不正确的是( )
| A. | 聚乙烯塑料制品可用于食品的包装 | |
| B. | 利用碳酸酯聚合材料生产一次性饭盒可以减少对环境产生的白色污染 | |
| C. | 汽车尾气中的NO、CO等是汽油和柴油的不完全燃烧产物 | |
| D. | 部分烷烃常用于家庭烹饪的燃料气 |
15.某原电池装置如右图所示,电池总反应为2Ag+Cl2=2AgCl.下列说法正确的是( )


| A. | 正极反应为AgCl+e-═Ag+Cl- | |
| B. | 当电路中转移0.01mole-时,交换膜左侧溶液中约减少0.02mol离子 | |
| C. | 若用NaCl溶液代替盐酸,则电池总反应随之改变 | |
| D. | 放电时,交换膜右侧中有大量白色沉淀生成 |
2.关于下列各实验装置的叙述中,不正确的是( )
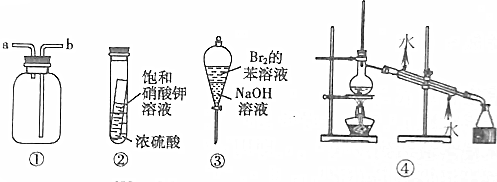

| A. | 装置①可用于收集H2、NH3、CO2、Cl2、HCl、NO2等气体 | |
| B. | 实验②放置一段时间后,小试管内有晶体析出 | |
| C. | 实验③振荡后静置,上层溶液颜色变浅 | |
| D. | 实验④可用于分离饱和Na2CO3溶液和CH3COOC2H5 |
11. 纳米级Cu2O由于具有优良的催化性能而受到关注,下表为制取Cu2O的三种方法:
纳米级Cu2O由于具有优良的催化性能而受到关注,下表为制取Cu2O的三种方法:
(1)工业上常用方法Ⅱ和方法Ⅲ制取Cu2O而很少用方法Ⅰ,其原因是反应条件不易控制,若控温不当易生成Cu而使Cu2O产率降低.
(2)方法Ⅰ制备过程会产生有毒气体,每生成1g该有毒气体,能量变化a kJ,写出制备反应的热化学方程式2CuO(s)+C(s)=Cu2O(s)+CO(g)△H=+28akJ•mol-1.
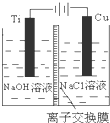
(3)方法Ⅱ采用离子交换膜控制电解液中OH-的浓度而制备纳米Cu2O,装置如图所示,该电池的阳极生成Cu2O反应式为2Cu-2e-+2OH-=Cu2O+H2O.
(4)方法Ⅲ为加热条件下用液态肼(N2H4)还原新制Cu(OH)2来制备纳米级Cu2O,同时放出N2.该制法的化学方程式为4Cu(OH)2+N2H4$\frac{\underline{\;\;△\;\;}}{\;}$2Cu2O+N2↑+6H2O.
(5)方法Ⅲ可以用甲醛稀溶液替代肼,但因反应温度较高而使部分产品颗粒过大,过滤(填操作名称)可分离出颗粒过大的Cu2O.
(6)在相同的密闭容器中,用方法Ⅱ和方法Ⅲ制得的Cu2O分别进行催化分解水的实验:2H2O(g)$\frac{\underline{\;光照\;}}{Cu_{2}O}$2H2(g)+O2(g)△H>0水蒸气的浓度(mol•L-1)随时间t(min)变化如下表:
可以判断:实验①的前20 min的平均反应速率 ν(O2)=3.5×10-5 mol•L-1 min-1;实验温度T1<T2(填“>”、“<”);催化剂的催化效率:实验①<实验②(填“>”、“<”).
 纳米级Cu2O由于具有优良的催化性能而受到关注,下表为制取Cu2O的三种方法:
纳米级Cu2O由于具有优良的催化性能而受到关注,下表为制取Cu2O的三种方法:| 方法Ⅰ | 用炭粉在高温条件下还原CuO |
| 方法Ⅱ | 电解法:2Cu+H2O $\frac{\underline{\;电解\;}}{\;}$Cu2O+H2↑ |
| 方法Ⅲ | 用肼(N2H4)还原新制Cu(OH)2 |
(2)方法Ⅰ制备过程会产生有毒气体,每生成1g该有毒气体,能量变化a kJ,写出制备反应的热化学方程式2CuO(s)+C(s)=Cu2O(s)+CO(g)△H=+28akJ•mol-1.
(3)方法Ⅱ采用离子交换膜控制电解液中OH-的浓度而制备纳米Cu2O,装置如图所示,该电池的阳极生成Cu2O反应式为2Cu-2e-+2OH-=Cu2O+H2O.
(4)方法Ⅲ为加热条件下用液态肼(N2H4)还原新制Cu(OH)2来制备纳米级Cu2O,同时放出N2.该制法的化学方程式为4Cu(OH)2+N2H4$\frac{\underline{\;\;△\;\;}}{\;}$2Cu2O+N2↑+6H2O.
(5)方法Ⅲ可以用甲醛稀溶液替代肼,但因反应温度较高而使部分产品颗粒过大,过滤(填操作名称)可分离出颗粒过大的Cu2O.
(6)在相同的密闭容器中,用方法Ⅱ和方法Ⅲ制得的Cu2O分别进行催化分解水的实验:2H2O(g)$\frac{\underline{\;光照\;}}{Cu_{2}O}$2H2(g)+O2(g)△H>0水蒸气的浓度(mol•L-1)随时间t(min)变化如下表:
| 序号 | 温度 | 0 | 10 | 20 | 30 | 40 | 50 |
| ① | T1 | 0.050 | 0.0492 | 0.0486 | 0.0482 | 0.0480 | 0.0480 |
| ② | T1 | 0.050 | 0.0488 | 0.0484 | 0.0480 | 0.0480 | 0.0480 |
| ③ | T2 | 0.10 | 0.094 | 0.090 | 0.090 | 0.090 | 0.090 |
8.25℃时,5种银盐的溶度积常数(Ksp)分别是:
下列说法正确的是( )
| AgCl | Ag2SO4 | Ag2S | AgBr | AgI |
| 1.8×10-10 | 1.4×10-5 | 6.3×10-50 | 7.7×10-13 | 8.51×10-16 |
| A. | 氯化银、溴化银和碘化银的溶解度依次增大 | |
| B. | 将硫酸银溶解于水后,向其中加入少量硫化钠溶液,不能得到黑色沉淀 | |
| C. | 在5mL1.8×10-5 mol/L的NaCl溶液中,加入1滴(1mL约20滴)0.1 mol/L的AgNO3溶液,不能观察到白色沉淀 | |
| D. | 将浅黄色溴化银固体浸泡在饱和氯化钠溶液中,可以有少量白色固体生成 |
9.原子序数逐渐增大的元素A、B、C、D、E、F的有关信息如下:
根据以上表格信息回答:
(1)元素F在周期表中的位置是第四周期IB族,E形成的低价离子的电子排布式为1s22s22p63s23p63d10.
(2)A、C的氢化物沸点较高的是(用所形成的氢化物表示)H2O,A、B、C的第一电离能大小顺序是(用元素符号表示)N>O>C.
(3)A与氢元素形成的A2H2含有的σ键、π键数目之比为3:2.
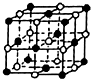
(4)KCl的晶胞如图:“●K,○Cl”,则该晶胞中含K+为4个,已知晶胞参数为:629.8pm(1pm=10-12m),求KCl晶体的密度为$\frac{4×(39+35.5)}{6.02×1{0}^{23}×(629.8×1{0}^{-10})^{3}}$g/cm3(只写出表达式,不要求计算结果).
(5)用惰性电极电解FCl2溶液时,在阴极除了析出红色固体外,还析出白色固体,经检验白色固体为FCl,请写出析出白色固体的阴极反应式Cu2++Cl-+e-=CuCl.
| 代号 | 信息 |
| A | 原子最外层电子数为内层电子数的2倍 |
| C | 形成的一种单质可抵御紫外线对地球生物的伤害 |
| D | 是一种非金属元素,属于卤族之一,形成的气体常温常压下为黄绿色 |
| E | 单质是生活中使用最广泛的金属 |
| F | 形成的一种化合物可用于醛基的检验 |
(1)元素F在周期表中的位置是第四周期IB族,E形成的低价离子的电子排布式为1s22s22p63s23p63d10.
(2)A、C的氢化物沸点较高的是(用所形成的氢化物表示)H2O,A、B、C的第一电离能大小顺序是(用元素符号表示)N>O>C.
(3)A与氢元素形成的A2H2含有的σ键、π键数目之比为3:2.
(4)KCl的晶胞如图:“●K,○Cl”,则该晶胞中含K+为4个,已知晶胞参数为:629.8pm(1pm=10-12m),求KCl晶体的密度为$\frac{4×(39+35.5)}{6.02×1{0}^{23}×(629.8×1{0}^{-10})^{3}}$g/cm3(只写出表达式,不要求计算结果).

(5)用惰性电极电解FCl2溶液时,在阴极除了析出红色固体外,还析出白色固体,经检验白色固体为FCl,请写出析出白色固体的阴极反应式Cu2++Cl-+e-=CuCl.