题目内容
14.某元素的一种同位素X的原子质量数为A,含N个中子,它与1H原子组成HmX分子.在a g HmX中所含质子的物质的量是( )| A. | a×(A-N+m)/(A+m)mol | B. | a×(A-N)/Amol | C. | a×(A-N)/(A+m)mol | D. | a×(A-N+m)/Amol |
分析 根据质子数=质量数-中子数计算X原子质子数,进而计算每个HmX分子含有质子数,根据n=$\frac{m}{M}$计算HmX的物质的量,结合每个分子含有质子数计算.
解答 解:某元素的一种同位素X的原子质量数为A,含N个中子,则质子数为(A-N),则每个HmX分子含有质子数为(A-N+m),ag HmX的物质的量为$\frac{ag}{(m+A)g/mol}$=$\frac{a}{m+A}$mol,故含有质子物质的量为$\frac{a}{m+A}$mol×(A-N+m)=$\frac{a}{m+A}$(A-N+m) mol,故选A.
点评 本题考查物质的量有关计算、原子结构,比较基础,属于字母型计算,一定程度上增大计算难度.

练习册系列答案
相关题目
4.一种碳纳米管能够吸附氢气,可做二次电池的碳电极(如图所示),该电池的电解质溶液是6mol/L溶液,下列说法中,错误的是( )
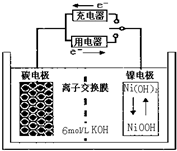

| A. | 充电时碳电极上发生还原反应 | |
| B. | 充电时Ni电极与电源的正极相连 | |
| C. | 放电时碳电极反应为H2-2e-=2H+ | |
| D. | 放电时Ni电极反应为Na(OH)+H2O+e-=Ni(OH)2+OH- |
5.在T℃时,铬酸银(Ag2CrO4)在水溶液中的沉淀溶解平衡曲线如图所示.下列说法中不正确的是( ) 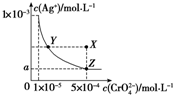

| A. | T℃时,在Y点和Z点,Ag2CrO4的Ksp相等 | |
| B. | 向饱和AgCrO4溶液中加入固体K2CrO4不能使溶液由Y点变为X点 | |
| C. | T℃时,Ag2CrO4的Ksp为1×10-8 | |
| D. | 图中a=$\sqrt{2}$×10-4 |
2.下列是对一些分子中共价键的描述,其中不正确的是( )
| A. | HCl分子中的共价键是由H原子的1s轨道和Cl原子未成对电子的3p轨道形成的s-pσ键 | |
| B. | 石墨晶体中碳原子的杂化轨道类型为sp2,碳原子间只存在sp2-sp2σ键 | |
| C. | H2O分子中的共价键是由O原子的sp3杂化轨道和H原子的s轨道形成的s-sp3σ键 | |
| D. | N2分子中的共价键是由2个N原子各自用3个p轨道形成的3个p-pπ键 |
3.把Cl2通入含22g NaBr的溶液中,反应后加热,烘干得到固体13.1g,则此固体成分为( )
| A. | NaCl | B. | NaCl和NaBr | C. | NaBr | D. | 无法确定 |
10.节能减排是中国转型发展的必经之路,工业生产中联合生产是实现节能减排的重要措施.下图是几种工业生产的联合生产工艺:

请回答下列问题:
(1)装置甲为电解池(惰性电极),根据图示转化关系可知:A为Cl2(填化学式),阴极反应式为2H++2e-=H2↑.
(2)装置丙的反应物为Ti,而装置戊的生成物为Ti,这两个装置在该联合生产中并不矛盾,原因是进入装置丙的Ti含有的杂质较多,从装置戊中出来的Ti较为纯净
装置戊进行反应时需要的环境为C(填字母序号).
A.HCl气体氛围中 B.空气氛围中 C.氩气氛围中 D.水中
(3)装置乙中发生的是工业合成甲醇的反应:CO(g)+2H2(g)=CH3OH(g)△H<0.
①该反应在不同温度下的化学平衡常数(K)如下表:
符合表中的平衡常数x的数值是B(填字母序号).
A.0 B.0.012 C.32.081 D.100
②若装置乙为容积固定的密闭容器,不同时间段各物质的浓度如下表:
反应从2min到4min之间,H2的平均反应速率为0.3mol•L-1•min-1.反应达到平衡时CO的转化率为62.5%.反应在第2min时改变了反应条件,改变的条件可能是A(填字母序号).
A使用催化剂 B降低温度C增加H2的浓度
(4)装置己可以看作燃料电池,该燃料电池的负极反应式为CH3OH+8OH--6e-=CO32-+6H2O.

请回答下列问题:
(1)装置甲为电解池(惰性电极),根据图示转化关系可知:A为Cl2(填化学式),阴极反应式为2H++2e-=H2↑.
(2)装置丙的反应物为Ti,而装置戊的生成物为Ti,这两个装置在该联合生产中并不矛盾,原因是进入装置丙的Ti含有的杂质较多,从装置戊中出来的Ti较为纯净
装置戊进行反应时需要的环境为C(填字母序号).
A.HCl气体氛围中 B.空气氛围中 C.氩气氛围中 D.水中
(3)装置乙中发生的是工业合成甲醇的反应:CO(g)+2H2(g)=CH3OH(g)△H<0.
①该反应在不同温度下的化学平衡常数(K)如下表:
| 温度/℃ | 250 | 350 |
| K | 2.041 | x |
A.0 B.0.012 C.32.081 D.100
②若装置乙为容积固定的密闭容器,不同时间段各物质的浓度如下表:
| c(CO)/mol•L-1 | c(H2)/mol•L-1 | c(CH3OH)/mol•L-1 | |
| 0min | 0.8mol•L-1 | 1.6mol•L-1 | 0 |
| 2min | 0.6mol•L-1 | y | 0.2mol•L-1 |
| 4min | 0.3mol•L-1 | 0.6mol•L-1 | 0.5mol•L-1 |
| 6min | 0.3mol•L-1 | 0.6mol•L-1 | 0.5mol•L-1 |
A使用催化剂 B降低温度C增加H2的浓度
(4)装置己可以看作燃料电池,该燃料电池的负极反应式为CH3OH+8OH--6e-=CO32-+6H2O.
8.化学与社会、生活、生产密切相关.对下列现象或事实的解释正确的是( )
| 选项 | 现象或事实 | 解释 |
| A | 明矾用于净水 | 明矾具有消毒杀菌的作用 |
| B | 含硫煤中加入适量石灰石可减少对大气的污染 | 使煤燃烧产生的SO2最终生成CaSO4 |
| C | 钢铁在海水中比在河水中更易腐蚀 | 海水中含氧量高于河水 |
| D | “地沟油”可以用来制生物柴油 | 其主要成分和从石油中提取的柴油类似 |
| A. | A | B. | B | C. | C | D. | D |




