题目内容
12.两种气态烃以任意比例混合,在101kPa、105℃时1L该混合烃与9L氧气混合,充分燃烧后恢复到原状态,所得气体体积仍是10L.下列各组混合烃中符合此条件的是( )| A. | CH4 C2H4 | B. | CH4 C3H6 | C. | C2H6 C3H4 | D. | C2H2 C3H6 |
分析 有机物燃烧前后体积不变,可设有机物的平均式为CxHy,根据燃烧的方程式计算分子组成特点,进而进行推断.
解答 解:设有机物的平均式为CxHy,则有:CxHy+(x+$\frac{y}{4}$)O2→xCO2+$\frac{y}{2}$H2O,有机物燃烧前后体积不变,则
1+x+$\frac{y}{4}$=x+$\frac{y}{2}$,y=4,
即混合气中平均含有H原子数为4,
A.CH4、C2H4中H原子数都为4,平均值为4,符合题意,故A选;
B.CH4、C3H6中H原子数分别为4、6.平均值不可能为4,故B不选;
C.C2H6 C3H4中H原子数都为6、4,平均值不可能为4,故C不选;
D.C2H2、C3H6H原子数分别为2、6,只有1:1混合才能使平均值为4,不符合以任意比例混合的要求,故D不选.
故选:A.
点评 本题考查有机物的确定,题目难度中等,注意根据有机物燃烧的方程式,用平均值法计算.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
17.X、Y、Z都是第三周期元素,核电荷数依次增大,X的氧化物对应水化物是强碱,Z的原子半径在该周期中最小.据此判断下列说法正确( )
| A. | X是第IA元素,Z是第ⅦA元素 | |
| B. | 元素X、Z形成的化合物是共价化合物 | |
| C. | Y一定是金属元素 | |
| D. | Z的最高价氧化物对应的水化物是弱酸 |
3.现代家居装修材料中,普遍存在着甲醛、苯及苯的同系物等有毒物质,如果不注意处理就会对人体产生极大的危害.按照有机物官能团的分类,甲醛属于醛.下面各项对有机物的分类方法与此方法相同的是( )
| A. | 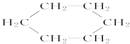 属于环状化合物 属于环状化合物 | B. |  属于卤代烃 属于卤代烃 | ||
| C. |  属于链状化合物 属于链状化合物 | D. | 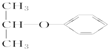 属于醚 属于醚 |
20.以下实验中能够获得成功的是( )
| A. | 将乙烷和氯气的混合气放在光照条件下反应制备氯乙烷(C2H5Cl) | |
| B. | 将乙醇迅速加热至170摄氏度制乙烯 | |
| C. | 将还原铁粉、液溴和苯混合制溴苯 | |
| D. | 检验氯代烃中含氯,加NaOH溶液加热后,用稀硫酸酸化,再检验 |
7. 向甲、乙、丙三个密闭容器中充入一定量的A和B,发生反应:A(g)+xB(g)?2C(g).各容器的反应温度、反应物起始量,反应过程中C的浓度随时间变化关系分别如表和如图表示:下列说法正确的是( )
向甲、乙、丙三个密闭容器中充入一定量的A和B,发生反应:A(g)+xB(g)?2C(g).各容器的反应温度、反应物起始量,反应过程中C的浓度随时间变化关系分别如表和如图表示:下列说法正确的是( )
 向甲、乙、丙三个密闭容器中充入一定量的A和B,发生反应:A(g)+xB(g)?2C(g).各容器的反应温度、反应物起始量,反应过程中C的浓度随时间变化关系分别如表和如图表示:下列说法正确的是( )
向甲、乙、丙三个密闭容器中充入一定量的A和B,发生反应:A(g)+xB(g)?2C(g).各容器的反应温度、反应物起始量,反应过程中C的浓度随时间变化关系分别如表和如图表示:下列说法正确的是( )| 容器 | 甲 | 乙 | 丙 |
| 容积 | 0.5L | 0.5L | 1.0L |
| 温度/℃ | T1 | T2 | T2 |
| 反应物 起始量 | 1.5molA 0.5molB | 1.5molA 0.5molB | 6.0molA 2.0molB |
| A. | 10min内甲容器中反应的平均速率v(A)=0.025mol/(L•min) | |
| B. | 由图可知:T1<T2,且该反应为吸热反应 | |
| C. | x=1,若平衡时保持温度不变,改变容器体积平衡移动 | |
| D. | T1℃,起始时甲容器中充入0.5molA、1.5molB,平衡时A的转化率为75% |
17.下列溶液中的Cl-浓度与50mL 1mol•L-1 MgCl2溶液中的Cl-浓度相等的是( )
| A. | 150 mL 1 mol•L-1 NaCl溶液 | B. | 75 mL 2 mol•L-1CaCl2溶液 | ||
| C. | 150 mL 2 mol•L-1 KCl溶液 | D. | 75 mL 1 mol•L-1AlCl3溶液 |
2.下列溶液中微粒的物质的量浓度关系正确的是( )
| A. | 已知H2C2O4为二元弱酸,则Na2C2O4溶液:c(OH- )=c(H+ )+c(H2C2O4-)+c(H2C2O4) | |
| B. | 等体积、等物质的量浓度的NaX和弱酸HX混合:c(Na+)=c(X-)>c(OH-)=c(H+) | |
| C. | 常温下,将25mL0.2mol/L的盐酸与100mL0.1mol/L的氨水混合,所得溶液中:c(Cl-)>c(NH4+)>c(NH3•H2O)>c(OH-)>c(H+) | |
| D. | 将0.1mol/L的Na2S溶液与0.1mol/L的NaHS溶液等体积混合,所得溶液中:2c(S2-)+c(OH-)+c(HS-)=c(H+)+c(Na+) |

