��Ŀ����
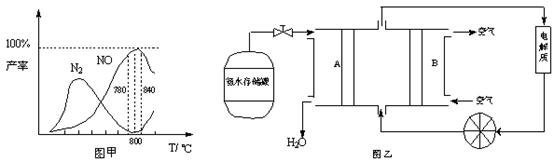
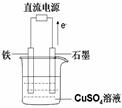
��ͼ��һ���Ҵ�ȼ�ϵ�ع���ʱ��ʾ��ͼ���ҳ��е������缫һ����ʯī�缫��һ�������缫������ʱM��N�����缫�������������٣���ش��������⣺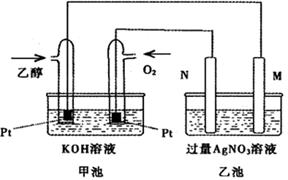
��1��M�缫�IJ����� ���缫������ �������Ҵ��IJ��缫�ĵ缫��Ӧ
ʽΪ ��д���ҳ��з����Ļ�ѧ��Ӧ�����ӷ���ʽ�� ��
��2���ڴ˹����У��ҳ���ijһ�缫����������4��32gʱ���׳�����������������Ϊ L����״���£�������ʱ�ҳ���Һ�����Ϊ400mL�����ҳ�����Һ��pHΪ ��
��3�����ڳ��³�ѹ�£�1g C2H5OHȼ������CO2��Һ̬H2Oʱ�ų�29��71kJ��������ʾ�÷�Ӧ���Ȼ�ѧ����ʽΪ ��
��4������Ҳ��һ�ֺܺõ������Դ���̲��ں��ġ���ȼ�����Ǹ�ѹ���γɵ��������ļ���ˮ������塣��������ȼ�յ��Ȼ�ѧ����ʽΪ��CH4(g)��2O2(g)��CO2(g)��2H2O(l) ��H����890��3 kJ��mol��356g����ȼ����(������ʽΪCH4��9H2O)�ͷŵļ���������ȫȼ������Һ̬ˮ���ų�������Ϊ kJ��
��1���� ���� C2H5OH��12e+16OH��=2CO32��+11H2O 4Ag++2H2O 4Ag+4H++O2����
4Ag+4H++O2����
��2��0��224 1 ��3��C2H5OH��l��+3O2��g�� 2CO2��g��+3H2O��l����H=��1366��7kJ/mol ��4��1780��6
���������������1����ͼ�ɿ���������ȼ�ϵ�ء�����ԭ��ء������ǵ��ء����ڼ׳���˵��ͨ���Ҵ��ĵ缫ʽ������ͨ�������ĵ缫�������������ҳ���˵��M��������N���������ҳ��е������缫һ����ʯī�缫��һ�������缫������ʱM��N�����缫�������������٣�˵�����缫��������M����ʯī�缫��������N��������Ϊ������缫���������ͻᷢ��������Ӧ�����������١������Ҵ��IJ��缫�ĵ缫��Ӧ��C2H5OH��12e+16OH��=2CO32��+11H2O���ҳؾ��ǵ����������Һ�������Ļ�ѧ��Ӧ�����ӷ���ʽ��4Ag++2H2O 4Ag+4H++O2������2���������պϻ�·�е���ת����Ŀ��ȡ�n(Ag)=m/M=4��32g��108g/mol=0��04mol��n(e-)=0��04mol������n(O2)=0��04mol��4=0��01mol��y��Ϊn=V/VM,����V=n��VM=0��01mol��22��4mol/L=0��224L����Ϊn(Ag)=n(H+)=0��04mol��V(aq)=0��4L����C(H+)=n/V��aq��=0��04mol��0��4L=0��1mol/L����PH=1��3���Ҵ�����Է���������46�����ڳ��³�ѹ�£�1g C2H5OHȼ������CO2��Һ̬H2Oʱ�ų�29��71kJ������46g�Ҵ�1molȼ������CO2��Һ̬H2Oʱ�ų�����46��29��71kJ=1366��7kJ����ʾ�÷�Ӧ���Ȼ�ѧ����ʽΪ��C2H5OH��l��+3O2��g��
4Ag+4H++O2������2���������պϻ�·�е���ת����Ŀ��ȡ�n(Ag)=m/M=4��32g��108g/mol=0��04mol��n(e-)=0��04mol������n(O2)=0��04mol��4=0��01mol��y��Ϊn=V/VM,����V=n��VM=0��01mol��22��4mol/L=0��224L����Ϊn(Ag)=n(H+)=0��04mol��V(aq)=0��4L����C(H+)=n/V��aq��=0��04mol��0��4L=0��1mol/L����PH=1��3���Ҵ�����Է���������46�����ڳ��³�ѹ�£�1g C2H5OHȼ������CO2��Һ̬H2Oʱ�ų�29��71kJ������46g�Ҵ�1molȼ������CO2��Һ̬H2Oʱ�ų�����46��29��71kJ=1366��7kJ����ʾ�÷�Ӧ���Ȼ�ѧ����ʽΪ��C2H5OH��l��+3O2��g�� 2CO2��g��+3H2O��l����H=��1366��7kJ/mol ��4����ȼ����Է�������Ϊ178��n(��ȼ��)=356g��108g/mol=2mol������ȫȼ������Һ̬ˮ���ų�������Ϊ2mol��890��3 kJ��mol=1780��6KJ
����ԭ��ء����ؼ��Ȼ�ѧ����ʽ����д��֪ʶ��

��֪������Һ��CrO42���Ի�ɫ��Cr2O72-�ԳȺ�ɫ
��PbCrO4������ˮ��Ҳ������ǿ��
��H+(aq��+OH-��aq��=H2O(l���� ��H=" ��a" KJ/mol
3Cl2��g��+2Cr3+��aq��+16OH-(aq��=2CrO42-��aq��+6Cl-��aq��+8H2O(l)����H="��b" KJ/mol
2CrO42-��aq��+2H+(aq��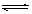 Cr2O72-��aq��+H2O(l������H="��c" KJ/mol
Cr2O72-��aq��+H2O(l������H="��c" KJ/mol
ƽ�ⳣ��K=9��5��104 ������a��b��c������0��
��������Ӧ�ݣ�ȡ50mL��Һ�������飬���ֲⶨ�������£�
| ʱ�䣨s�� | 0 | 0��01 | 0��02 | 0��03 | 0��04 |
| n ��CrO42������mol�� | 0��01 | 8��0��10-4 | 5��4��10-4 | 5��0��10-4 | |
| n ��Cr2O72������mol�� | 0 | | 4��73��10-3 | | 4��75��10-3 |
�Իش��������⣺
��1��0.02s��0.03s֮����Cr2O72-��ʾ�÷�Ӧ��ƽ����Ӧ����Ϊ
����˵����ȷ�ģ� ��
A��0.03sʱV����CrO42����=2V�棨Cr2O72����
B����ҺpHֵ����˵���÷�Ӧ�Ѵ�ƽ��״̬
C����Һ��c��CrO42������c��Cr2O72����=2:1ʱ�÷�Ӧ�Ѵ�ƽ��״̬
D����Ӧ����2��5��10-3c KJʱCrO42����ת����Ϊ50��
E�����¸÷�Ӧƽ�ⳣ�����
F��0��04sʱ����������Pb��NO3)2 ��ʹ��Һ�ɳ�ɫ��Ϊ��ɫ
��3��0��03sʱ��Һ��pH=
��4����֪����������Cr2O72����Cl-����ΪCl2����������ԭΪCr3+Ϊ���ȷ�Ӧ����д���÷�Ӧ���Ȼ�ѧ����ʽ��
���£��ݻ�Ϊ1 L���������£�����Է�������ת�����䷴Ӧ���̺�������ϵ��ͼ1��ʾ(��֪��2SO2(g)��O2(g) 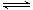 2SO3(g) ��H����196.6 kJ��mol��1)����ش��������⣺
2SO3(g) ��H����196.6 kJ��mol��1)����ش��������⣺
(1)д���ܱ�ʾ���ȼ���ȵ��Ȼ�ѧ����ʽ��______________________��
(2)��H2��__________kJ��mol��1��
��.��ҵ�ϳ����ô�����Ҵ��ϳ��л��ܼ�����������
CH3COOH(l)��C2H5OH(l)  CH3COOC2H5(l)��H2O(l) ��H����8.62 kJ��mol��1
CH3COOC2H5(l)��H2O(l) ��H����8.62 kJ��mol��1
��֪CH3COOH��C2H5OH��CH3COOC2H5�ķе�����Ϊ118 �桢78 ���77 �档������������ͬʱ��ij�о�С������˶��ʵ�飬ʵ������ͼ��ʾ��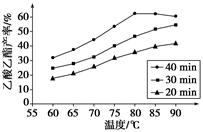
(1)���о�С���ʵ��Ŀ����___________________________________��
(2)60 ���·�Ӧ40 min��70 ���·�Ӧ20 min��ȣ�ǰ�ߵ�ƽ����Ӧ����________����(�С�ڡ��������ڡ����ڡ�)��
(3)��ͼ��ʾ����Ӧʱ��Ϊ40 min���¶ȳ���80 ��ʱ���������������½���ԭ�������_________________________________(д������)��
��.ú�����г����о���ͬ�¶���ƽ�ⳣ����Ͷ�ϱȼ���ֵ�����⡣
��֪��CO(g)��H2O(g) 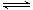 H2(g)��CO2(g)ƽ�ⳣ�����¶ȵı仯���±���
H2(g)��CO2(g)ƽ�ⳣ�����¶ȵı仯���±���
| �¶�/�� | 400 | 500 | 800 |
| ƽ�ⳣ��K | 9.94 | 9 | 1 |
�Իش��������⣺
(1)��800 �淢��������Ӧ���Ա��е����ʵ���Ͷ����ݷ�Ӧ��������������Ӧ�����ƶ�����________(ѡ�A��B��C��D��E��)��
| | n(CO) | n(H2O) | n(H2) | n(CO2) |
| A | 1 | 5 | 2 | 3 |
| B | 2 | 2 | 1 | 1 |
| C | 3 | 3 | 0 | 0 |
| D | 0.5 | 2 | 1 | 1 |
| E | 3 | 1 | 2 | 1 |
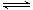 2CO(g)ƽ�ⳣ��ΪK��
2CO(g)ƽ�ⳣ��ΪK����C(s)��H2O(g)
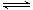 CO(g)��H2(g) ƽ�ⳣ��ΪK1��
CO(g)��H2(g) ƽ�ⳣ��ΪK1����CO(g)��H2O(g)
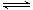 H2(g)��CO2(g) ƽ�ⳣ��ΪK2��
H2(g)��CO2(g) ƽ�ⳣ��ΪK2����K��K1��K2֮��Ĺ�ϵ��______________________________________��
 2NH3(g)����H����92.4 kJ/mol
2NH3(g)����H����92.4 kJ/mol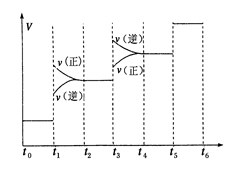
 2SO3(g)��д���÷�Ӧ�Ļ�ѧƽ�ⳣ������ʽ��
2SO3(g)��д���÷�Ӧ�Ļ�ѧƽ�ⳣ������ʽ�� 
 CH3OH(g)+H2O(g) ��H1 �ش��������⡣
CH3OH(g)+H2O(g) ��H1 �ش��������⡣ CO(g) + 3H2(g)��һ���¶��£���2 mol CH4��4 mol H2Oͨ���ݻ�Ϊ10L���ܱշ�Ӧ���У���Ӧ��CO�����ʵ���Ũ�ȵı仯�����ͼ��ʾ����ش��������⣺
CO(g) + 3H2(g)��һ���¶��£���2 mol CH4��4 mol H2Oͨ���ݻ�Ϊ10L���ܱշ�Ӧ���У���Ӧ��CO�����ʵ���Ũ�ȵı仯�����ͼ��ʾ����ش��������⣺
 4NO(g)+6H2O(g) ��H =" ��905" kJ/mol ������Ӧ
4NO(g)+6H2O(g) ��H =" ��905" kJ/mol ������Ӧ