题目内容
【题目】氮的化合物既是一种资源,也会给环境造成危害。
I.氨气是一种重要的化工原料。
(1)NH3与CO2在120℃,催化剂作用下反应生成尿素:CO2(g)+2NH3(g)![]() CO(NH2)2(s)+H2O(g),△H=-xkJ/mol(x>0),其他相关数据如表:
CO(NH2)2(s)+H2O(g),△H=-xkJ/mol(x>0),其他相关数据如表:
物质 | NH3(g) | CO2(g) | CO(NH2)2(s) | H2O(g) |
1mol分子中的化学键断裂时需要吸收的能量/kJ | a | b | z | d |
则表中z(用x、a、b、d表示)的大小为___。
(2)120℃时,在2L密闭反应容器中充入3molCO2与NH3的混合气体,混合气体中NH3的体积分数随反应时间变化关系如图2所示,该反应60s内CO2的平均反应速率为___。

下列能使正反应的化学反应速率加快的措施有___。
①及时分离出尿素 ②升高温度 ③向密闭定容容器中再充入CO2 ④降低温度
Ⅱ.氮的氧化物会污染环境。目前,硝酸厂尾气治理可采用NH3与NO在催化剂存在的条件下作用,将污染物转化为无污染的物质。某研究小组拟验证NO能被氨气还原并计算其转化率(已知浓硫酸在常温下不氧化NO气体)。
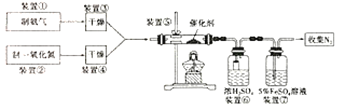


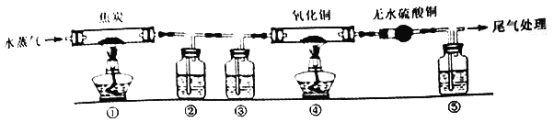
(3)写出装置⑤中反应的化学方程式___;
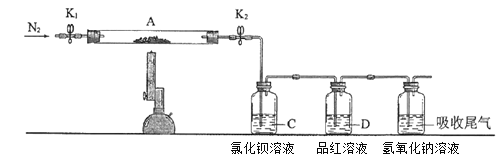
(4)装置①和装置②如图4,仪器A中盛放的药品名称为___。装置②中,先在试管中加入2-3粒石灰石,注入适量稀硝酸,反应一段时间后,再塞上带有细铜丝的胶塞进行后续反应,加入石灰石的作用是___。
(5)装置⑥中,小段玻璃管的作用是___;装置⑦的作用是除去NO,NO与FeSO4溶液反应形成棕色[Fe(NO)]SO4溶液,同时装置⑦还用来检验氨气是否除尽,若氨气未除尽,可观察到的实验现象是___。
【答案】x-d+b+2a 0.0047mol/(Ls) ②③ 4NH3+6NO![]() 5N2+6H2O 浓氨水 产生CO2,排出装置中的空气,防止NO被氧化 防倒吸 溶液变浑浊
5N2+6H2O 浓氨水 产生CO2,排出装置中的空气,防止NO被氧化 防倒吸 溶液变浑浊
【解析】
(1) △H=反应物的总键能-生成物的总键能。
(2)设参加反应的CO2物质的量为x,利用三段式建立关系式,求出x,从而可求出该反应60s内CO2的平均反应速率。
①尿素呈固态,及时分离出尿素,对反应没有影响;
②升高温度,可加快反应速率;
③向密闭定容容器中再充入CO2,增大反应物浓度,加快反应速率;
④降低温度,减慢反应速率。
(3)装置⑤中,NH3、NO在催化剂作用下反应,生成N2和水。
(4)装置①利用浓氨水滴入生石灰中制取氨气。装置②中,先在试管中加入2-3粒石灰石,注入适量稀硝酸,反应一段时间后,再塞上带有细铜丝的胶塞进行后续反应,由于NO易与空气中的O2反应,所以加入石灰石,排尽装置内的空气。
(5)装置⑥用于干燥气体,但NH3易被浓硫酸吸收产生倒吸;装置⑦的作用是除去NO,NO与FeSO4溶液反应形成棕色[Fe(NO)]SO4溶液,同时装置⑦还用来检验氨气是否除尽,若氨气未除尽,NH3会与FeSO4发生反应。
(1) △H=反应物的总键能-生成物的总键能,即-x=(2a+b)-(z+d),从而得出z=x-d+b+2a。答案为:x-d+b+2a;
(2)设参加反应的CO2物质的量为x,利用三段式建立关系式:
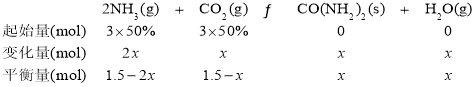
![]() ,x=
,x=![]() mol,该反应60s内CO2的平均反应速率为
mol,该反应60s内CO2的平均反应速率为 = 0.0047mol/(Ls)。答案为:0.0047mol/(Ls);
= 0.0047mol/(Ls)。答案为:0.0047mol/(Ls);
①尿素呈固态,及时分离出尿素,对反应没有影响,①不合题意;
②升高温度,可加快反应速率,②符合题意;
③向密闭定容容器中再充入CO2,增大反应物浓度,加快反应速率,③符合题意;
④降低温度,减慢反应速率,④不合题意;
故选②③。答案为:②③;
(3) 装置⑤中,NH3、NO在催化剂作用下反应,生成N2和水,反应的化学方程式4NH3+6NO![]() 5N2+6H2O。答案为:4NH3+6NO
5N2+6H2O。答案为:4NH3+6NO![]() 5N2+6H2O;
5N2+6H2O;
(4) 装置①利用浓氨水滴入生石灰中制取氨气,仪器A中盛放的药品名称为浓氨水。
装置②中,先在试管中加入2-3粒石灰石,注入适量稀硝酸,反应一段时间后,再塞上带有细铜丝的胶塞进行后续反应,由于NO易与空气中的O2反应,所以加入石灰石的作用是产生CO2,排出装置中的空气,防止NO被氧化。答案:浓氨水;产生CO2,排出装置中的空气,防止NO被氧化;
(5)装置⑥用于干燥气体,但NH3易被浓硫酸吸收而产生负压,所以小段玻璃管的作用是防倒吸;装置⑦的作用是除去NO,NO与FeSO4溶液反应形成棕色[Fe(NO)]SO4溶液,同时装置⑦还用来检验氨气是否除尽,若氨气未除尽,NH3会与FeSO4发生反应,可观察到的实验现象是溶液变浑浊。答案为:防倒吸;溶液变浑浊。

 口算题天天练系列答案
口算题天天练系列答案【题目】用如图所示实验装置探究铜丝与过量浓硫酸的反应。
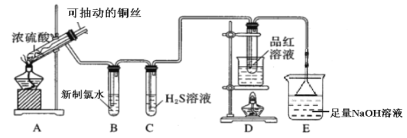
(1)写出A中发生反应的化学方程式__________。在此反应中,浓硫酸表现出来的性质有__________。(填字母序号)
A.强氧化性 B.酸性 C.吸水性 D.脱水性
(2)一段时间后,观察到B中溶液黄绿色褪去,B中反应的化学方程式为__________。C中的实验现象为__________。
(3)D中的实验现象是__________,一段时间后,点燃D处酒精灯,可以观察到__________。
(4)E装置中NaOH溶液的作用是__________。
(5)研究小组认为可以用H2O2溶液来验证E中溶液含有SO32-,进行了实验i。
实验序号 | 操作 | 现象 |
i | a. 取少量E中溶液,向其中加入适量H2O2溶液,振荡,观察。 | 无明显现象 |
b. 然后滴加__________,振荡,观察。 | 无明显现象 | |
c. 再滴加__________,振荡,观察。 | 白色沉淀 |
通过实验i可证明E中溶液含有SO32-,写出操作b、c中滴加的试剂是__________、__________。
(6)研究小组反思实验方案i不够严谨,设计了对比实验,证明了E中含有SO32-。该对比实验方案是__________。