题目内容
【题目】下列有关化学用语叙述中不正确的是( )
A.NH4H的电子式为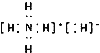 ,NH4H中的H-半径比锂离子半径大
,NH4H中的H-半径比锂离子半径大
B.NH4H晶体既有共价键又有离子键
C.N2的电子式:![]() ,二氧化碳分子的结构式为O-C-O
,二氧化碳分子的结构式为O-C-O
D.镁-24原子表示为![]() Mg,S原子的结构示意图
Mg,S原子的结构示意图![]()
【答案】C
【解析】
A.NH4H为离子化合物,由NH4+和H-构成,电子式为 ,NH4H中的H-与Li+电子层结构相同,但核电荷数比Li+小,所以H-半径大,A正确;
,NH4H中的H-与Li+电子层结构相同,但核电荷数比Li+小,所以H-半径大,A正确;
B.NH4H晶体中NH4+内N、H原子间形成共价键,NH4+与H-间形成离子键,B正确;
C.N2的电子式为![]() ,二氧化碳分子的结构式为O=C=O,C不正确;
,二氧化碳分子的结构式为O=C=O,C不正确;
D.镁-24表示镁原子的质量数为24,可表示为![]() Mg,S原子的结构示意图可表示为
Mg,S原子的结构示意图可表示为![]() ,D正确;
,D正确;
故选C。

【题目】实验室中某些气体的制取、收集及尾气处理装置如图所示(省略夹持和净化装置)。仅用此装置和表中提供的物质完成相关实验,最合理的选项是
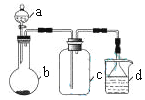
选项 | a中的物质 | b中的物质 | c中收集的气体 | d中的物质 |
A | 浓氨水 | CaO | NH3 | H2O |
B | 浓硫酸 | Na2SO3 | SO2 | NaOH溶液 |
C | 稀硝酸 | Cu | NO2 | H2O |
D | 浓盐酸 | MnO2 | Cl2 | NaOH溶液 |
【题目】氮的化合物既是一种资源,也会给环境造成危害。
I.氨气是一种重要的化工原料。
(1)NH3与CO2在120℃,催化剂作用下反应生成尿素:CO2(g)+2NH3(g)![]() CO(NH2)2(s)+H2O(g),△H=-xkJ/mol(x>0),其他相关数据如表:
CO(NH2)2(s)+H2O(g),△H=-xkJ/mol(x>0),其他相关数据如表:
物质 | NH3(g) | CO2(g) | CO(NH2)2(s) | H2O(g) |
1mol分子中的化学键断裂时需要吸收的能量/kJ | a | b | z | d |
则表中z(用x、a、b、d表示)的大小为___。
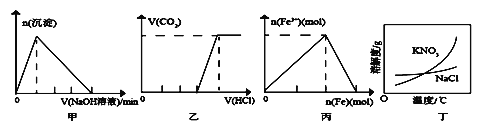
(2)120℃时,在2L密闭反应容器中充入3molCO2与NH3的混合气体,混合气体中NH3的体积分数随反应时间变化关系如图2所示,该反应60s内CO2的平均反应速率为___。

下列能使正反应的化学反应速率加快的措施有___。
①及时分离出尿素 ②升高温度 ③向密闭定容容器中再充入CO2 ④降低温度
Ⅱ.氮的氧化物会污染环境。目前,硝酸厂尾气治理可采用NH3与NO在催化剂存在的条件下作用,将污染物转化为无污染的物质。某研究小组拟验证NO能被氨气还原并计算其转化率(已知浓硫酸在常温下不氧化NO气体)。
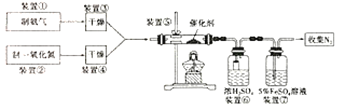


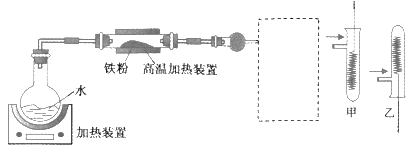
(3)写出装置⑤中反应的化学方程式___;
(4)装置①和装置②如图4,仪器A中盛放的药品名称为___。装置②中,先在试管中加入2-3粒石灰石,注入适量稀硝酸,反应一段时间后,再塞上带有细铜丝的胶塞进行后续反应,加入石灰石的作用是___。
(5)装置⑥中,小段玻璃管的作用是___;装置⑦的作用是除去NO,NO与FeSO4溶液反应形成棕色[Fe(NO)]SO4溶液,同时装置⑦还用来检验氨气是否除尽,若氨气未除尽,可观察到的实验现象是___。