题目内容
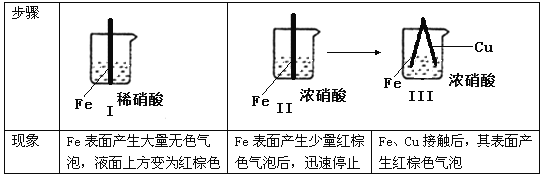
【题目】在处理胶片的废液中含有大量Ag+、Zn2+、Fe2+,某化学课外小组想从上述废液中回收银,并得到副产品硫酸亚铁,设计如下生产流程:
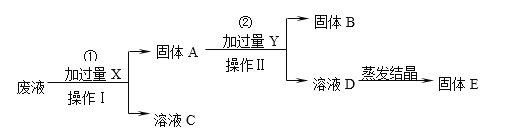
请回答:
⑴操作Ⅰ的名称是______,固体B的主要成分是______,X的化学式是______,Y的化学式是______。
⑵写出步骤②中反应的离子方程式_________________________________。
【答案】过滤 银 Fe H2SO4 2H++Fe=Fe2++H2↑
【解析】
先加入过量的铁粉,将银置换出来,再过滤,滤液C为锌离子和亚铁离子,固体A为Ag和Fe,固体A再加足量硫酸,铁粉溶解,银不溶解,再过滤,得到B为Ag,溶液D为硫酸亚铁和未反应的稀硫酸,最后得到固体E硫酸亚铁。
⑴操作Ⅰ是固体和溶液的分离,因此操作Ⅰ的名称是过滤,固体A为Ag和Fe,固体A再加足量硫酸,铁粉溶解,银不溶解,因此固体B的主要成分是Ag,混合离子先加入过量的铁粉,将银置换出来,再过滤,因此X的化学式是Fe,固体A为Ag和Fe,固体A再加足量硫酸,铁粉溶解,因此Y的化学式是H2SO4,故答案为:过滤;Ag;Fe;H2SO4。
⑵写出步骤②中反应的离子方程式2H++Fe=Fe2++H2↑,故答案为2H++Fe=Fe2++H2↑。

【题目】醇分子间脱水生成醚是制备简单醚的常用方法。用硫酸作为催化剂,在不同的温度下正丁醇和硫酸作用生成的产物会有不同,因此反应需严格控制温度。
主反应 ![]()
副反应 ![]()
主要实验装置如图所示
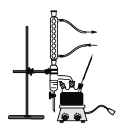
主要试剂及产物的部分性质如下表所示
名称 | 正丁醇 | 正丁醚 | 浓硫酸 |
相对分子质量 | 74 | 130 | 98 |
性状 | 无色液体 | 无色液体 | 无色液体 |
相对密度 | 0.8098 | 0.7689 | 1.84 |
沸点/℃ | 117.7 | 142.4 | 340 |
溶解度/(g/100ml水) | 7.7 | <0.5 |
实验步骤如下:
①在干燥的100mL三颈烧瓶中,放入14.8g正丁醇和4g(2.2mL)浓硫酸,摇动混合,并加入几粒沸石。按装置图,一瓶口装上温度计,温度计的水银球浸入液面以下。另一瓶口装上油水分离器(分水器),先在分水器中放置VmL水,然后将三颈烧瓶在电热套中加热,使瓶内液体微沸,开始回流。
②随反应的进行,分水器中液面增高,这是由于反应生成的水,以及未反应的正丁醇(在三颈烧瓶中会有二元或三元恒沸物)蒸出,经冷凝管冷凝后聚集于分水器内。继续加热到瓶内温度升高到135℃左右。分水器已全部被水充满时,表示反应已基本完成,约需1h。如继续加热,则溶液容易碳化变黑,并有大量副产物生成。
③反应物冷却后,把混合物连同分水器里的水一起倒入盛有一定量水的分液漏斗中,充分振荡,静置后,分出产物粗制正丁醚。用16mL5.0mol/L硫酸分2次洗涤,再用10mL水洗涤,然后加入无水氯化钙。将干燥后的产物注入蒸馏烧瓶中,收集139~142℃馏分,产量为5.6g。
请回答下列问题:
(1)在三颈烧瓶中加入几粒沸石,目的是____________。
(2)仪器a的名称是_____________。
(3)先在分水器中放置VmL水,已知分水器的容积为10mL,试计算VmL为_____mL(保留两位有效数字)。
(4)实验装置图中分水器的作用是________________________________。
(5)反应温度不易过高,溶液容易碳化变黑,并有大量副产物_____________生成。
(6)实验过程中需用5.0mol/L硫酸分2次洗涤正丁醚,用浓硫酸配制5.0mol/L硫酸溶液时,定容的操作方法为___________________________________。
(7)在③步骤中用10mL水洗涤的目的是_________。
(8)本实验最终获得5.6g正丁醚,则产率为_________(保留三位有效数字)。