题目内容
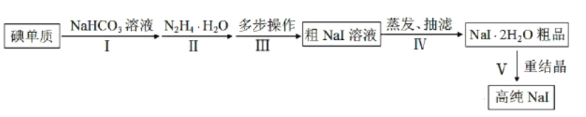
【题目】碘化钠在光学器件石油探测、安检、环境监测等领域有重要应用。某研究小组开发设计的制备高纯NaI的简化流程如图:
已知:
①I2(s)+I-(aq)![]() I
I![]() (aq)。
(aq)。
②水合肼(N2H4H2O)具有强还原性,可分别将碘的各种酸根和I2还原为I-,本身被氧化为无毒物质。
③NaI易溶于水,也易溶于酒精,在酒精中的溶解度随温度的升高增加不大。
请回答:
(1)步骤Ⅰ,I2与NaHCO3溶液发生歧化反应,生成物中含IO-和IO![]() 离子。
离子。
①I2与NaHCO3溶液反应适宜温度为40~70℃,则采用的加热方式为__。
②实验过程中,加少量NaI固体能使反应速率加快,其原因是__。
(2)步骤Ⅱ,水合肼与IO-反应的离子方程式为__。
(3)步骤Ⅲ,多步操作为:
①将步骤Ⅱ得到的pH为6.5~7的溶液调整pH值至9~10,在100℃下保温8h,得到溶液A;
②将溶液A的pH值调整至3~4,在70~80℃下保温4h,得溶液B;
③将溶液B的pH调整至6.5~7,得溶液C;
④在溶液C中加入活性炭,混合均匀后煮沸,静置10~24h后,过滤除杂得粗NaI溶液。
上述①②③操作中,调整pH值时依次加入的试剂为__。
A.NaOH B.HI C.NH3H2O D.高纯水
(4)步骤Ⅳ,采用改进的方案为用“减压蒸发”代替“常压蒸发”。
①“减压蒸发”需选用的仪器除了圆底烧瓶、蒸馏头、温度计、接收管、接收瓶之外,还有__。
A.直形冷凝管 B.球形冷凝管 C.烧杯 D.抽气泵
②采用“减压蒸发”的优点为__。
(5)将制备的NaI2H2O粗品以95%乙醇为溶剂进行重结晶。请给出合理的操作排序__。
加热95%乙醇→____→___→___→____→纯品(选填序号)。
①减压蒸发结晶 ②NaI2H2O粗品溶解 ③趁热过滤 ④真空干燥
【答案】水浴 因为NaI固体溶于水产生I-(aq)与I2(S)反应形成I![]() (aq),使固体I2溶解性增加,导致浓度增加,使与NaHCO3溶液反应的反应速率加快 N2H4·H2O+2IO-=N2↑+2I-+3H2O ABA AD 减压环境与外界空气隔绝,避免I-被氧化;降低压强,沸点降低,利于水的蒸 ②→①→③→④
(aq),使固体I2溶解性增加,导致浓度增加,使与NaHCO3溶液反应的反应速率加快 N2H4·H2O+2IO-=N2↑+2I-+3H2O ABA AD 减压环境与外界空气隔绝,避免I-被氧化;降低压强,沸点降低,利于水的蒸 ②→①→③→④
【解析】
(1)①为了控制温度在 ![]() ,可采用水浴加热。
,可采用水浴加热。
②![]() 在水中溶解度不大,加入
在水中溶解度不大,加入 ![]() 固体后因发生
固体后因发生 ![]() 而促进
而促进 ![]() 溶解,加快反应速率。
溶解,加快反应速率。
(2)![]() 具有强还原性,可以将
具有强还原性,可以将 ![]() 氧化成
氧化成 ![]() ,自身转变为无毒物质,则
,自身转变为无毒物质,则
![]()
![]()
![]() 价
价![]() 2×2
2×2
![]()
![]()
![]() 价
价![]()
![]()
利用氧还配平可得:![]() 。
。
(3)在①②③操作中,为了不引入杂质调节 ![]() 值应分别加
值应分别加 ![]() 、
、![]() 、
、![]() 溶液。
溶液。
(4)①减压蒸发是在低于大气压下进行蒸发操作,将二次蒸气经过冷凝器后排出,所以除列出仪器外,还需直形冷凝管和抽气泵。
②隔绝空气可以避免加热过程中 ![]() 被氧化;装置中气压低于大气压,
被氧化;装置中气压低于大气压,![]() 的沸点降低,有利于水的蒸发。
的沸点降低,有利于水的蒸发。
(5)由于 ![]() 易溶于酒精,且在酒精中的溶解度随温度变化不大,所在乙醇中进行重结晶。先加热溶剂乙醇,再溶解
易溶于酒精,且在酒精中的溶解度随温度变化不大,所在乙醇中进行重结晶。先加热溶剂乙醇,再溶解 ![]() ,减压蒸发结晶使
,减压蒸发结晶使 ![]() 析出,趁热过滤后在真空中干燥,避免
析出,趁热过滤后在真空中干燥,避免 ![]() 被氧化,操作顺序为③②④⑤。
被氧化,操作顺序为③②④⑤。

 初中学业考试导与练系列答案
初中学业考试导与练系列答案