题目内容
【题目】为了验证木炭可被浓硫酸氧化成CO2,选用如图所示装置(内含物质)进行实验。

(1)如按气流由左向右的流向,连接如图所示装置的正确顺序是_______(填字母)
(2)若实验检验出有CO2生成,则装置乙、丙中的现象分别为装置乙中______,装置丙中________。
(3)装置丁中酸性KMnO4溶液的作用是________。
(4)写出装置甲中所发生反应的化学方程式:________。
【答案】A;F;E;C;D;B 澄清石灰水变浑浊 品红溶液未褪色 吸收SO2 C+2H2SO4(浓)![]() CO2↑+2SO2↑+2H2O
CO2↑+2SO2↑+2H2O
【解析】
根据题中各装置特点及药品可知,甲为气体发生装置、乙为检验二氧化碳装置、丙为检验二氧化硫是否除尽装置、丁为除去二氧化硫的装置,据此分析解答。
(1)甲为浓硫酸与碳发生反应的装置,高锰酸钾可氧化二氧化硫,用酸性高锰酸钾溶液除SO2,再通过品红溶液不褪色确认SO2已除干净,验证木炭可被浓硫酸氧化成CO2,可通过二氧化碳能使澄清的石灰水变浑浊确认,所以装置连接顺序为:A→F→E→C→D→B;
(2)二氧化硫具有漂白性,二氧化硫能使品红褪色,丁装置用高锰酸钾酸性溶液除SO2,再通过品红溶液不褪色,证明二氧化硫已经除尽,若丙中品红褪色,则乙中的澄清的石灰水变浑浊,无法证明甲中反应生成了二氧化碳,因此若实验检验出有CO2生成,则装置乙、丙中的现象分别为装置乙中澄清石灰水变浑浊,装置丙中品红溶液未褪色;
(3)若证明有二氧化碳,需要先除去干扰气体二氧化硫,用高锰酸钾可以吸收二氧化硫;
(4)浓硫酸与木炭在加热条件下反应生成二氧化碳、二氧化硫和水,方程式为C+2H2SO4(浓)![]() CO2↑+2SO2↑+2H2O。
CO2↑+2SO2↑+2H2O。

【题目】Ⅰ、反应A(g)+B(g)![]() C(g)+D(g)过程中的能量变化如图所示,回答下列问题.
C(g)+D(g)过程中的能量变化如图所示,回答下列问题.
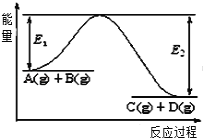
(1)该反应是_________反应(填“吸热”、“放热”)。
(2)当反应达到平衡时,升高温度,A的转化率_______(填“增大”、“减小”、“不变”)。
(3)反应体系中加入催化剂对反应热是否有影响?_____(填“有”、“无”),原因是____。
(4)在反应体系中加入催化剂,反应速率增大,E1的变化是:E1____(填“增大”、“减小”、“不变”)。
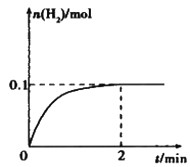
Ⅱ、五氯化磷(PCl5)是有机合成中重要的氯化剂,可以由三氯化磷(PCl3)氯化得到:PCl3(g)+Cl2(g) ![]() PCl5(g) △H=-0.930 kJmol-1 。某温度下,在容积恒定为2.0L的密闭容器中充入2.0 mol PCl3和1.0 mol Cl2,一段时间后反应达平衡状态,实验数据如下表所示:
PCl5(g) △H=-0.930 kJmol-1 。某温度下,在容积恒定为2.0L的密闭容器中充入2.0 mol PCl3和1.0 mol Cl2,一段时间后反应达平衡状态,实验数据如下表所示:
t/s | 0 | 50 | 150 | 250 | 350 |
n(PCl5)/mol | 0 | 0.24 | 0.36 | 0.40 | 0.40 |
(1)50~150s内的平均反应速率v(PCl3)=___________。
(2)该温度下,此反应的化学平衡常数的数值为___________。
(3)反应至250s时,该反应放出的热量为______________kJ。
(4)下列关于上述反应的说法中,正确的是__________(填字母序号)。
a.无论是否达平衡状态,混合气体的密度始终不变
b.300s时,升高温度,正、逆反应速率同时增大
c.350s时,向该密闭容器中充入氮气,平衡向正反应方向移动
d.相同条件下,若起始向该密闭容器中充入1.2molPCl3、0.5molCl2 和0.15mol PCl5,则反应向正反应方向进行