��Ŀ����
13��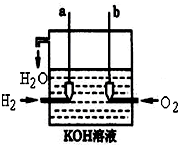 ��������������ɴ���ʹ�õ�����ȼ�ϵ����һ�����͵ĵ�أ��乹����ͼ��ʾ������Ϊ���̼�Ƴɣ�ͨ��������ɿ�϶�����������ӵ缫����ų���
��������������ɴ���ʹ�õ�����ȼ�ϵ����һ�����͵ĵ�أ��乹����ͼ��ʾ������Ϊ���̼�Ƴɣ�ͨ��������ɿ�϶�����������ӵ缫����ų�����a�Ǹ������缫��Ӧʽ��2H2-4e-+4OH-=4H2O��
��b�缫��Ӧʽ��O2+4e-+2H2O=4OH-��
������������ȼ�ϵ�������ȼ�ϣ���Ȼʹ�÷��㣬ȴ�ܵ���Դ�ͼ۸�����ƣ����õ�ȼ��������ijЩ̼�⻯�������飨��Ȼ���������͵ȣ���д��ͼ��H2����CH4ʱ���ɵļ���ȼ�ϵ����a���ĵ缫��ӦʽCH4+10OH--8e-=CO32-+7H2O����ʱ����ڵ��ܷ�Ӧ����ʽΪCH4+2O2+2OH-=CO32-+3H2O����Һ��PH��С������С�����䣩��
���� ������ȼ�ϵ���У�ԭ��ع���ʱ������ȼ�ϵ�ص��ܷ�ӦΪ2H2+O2=2H2O��ͨ��������һ��aΪ��Դ�ĸ���������������Ӧ���缫��ӦʽΪ��H2-2e-+2OH-=2H2O��
��ͨ��������һ��bΪԭ��ص��������缫��ӦʽΪ��O2+4e-+2H2O=4OH-��
���������ɼ����Ǽ����������Ӧ���ɶ�����̼��ˮ��������ԭ��Ӧ��ͼ�е������Һ�Ǽ�����Һ������ԭ��ص�ԭ�������Ԫ�ػ��ϼ۱仯����ʧ���ӵ����ʼ����ڸ���a����������Ӧ������������b������ԭ��Ӧ��
��� �⣺������ȼ�ϵ���У�ͨ��������һ��Ϊ��Դ�ĸ�����ͨ��������һ��Ϊԭ��ص����������ڵ������Һ�ʼ��ԣ����缫��ӦʽΪ��2H2-4e-+4OH-=4H2O��
�ʴ�Ϊ������2H2-4e-+4OH-=4H2O��
�������缫��ӦʽΪ��O2+4e-+2H2O=4OH-��
�ʴ�Ϊ��O2+4e-+2H2O=4OH-��
��ͼ��H2����CH4ʱ�����ɵļ���ȼ�ϵ���У�����ȼ�����ɶ�����̼��ˮ��������̼���������ط�Ӧ����̼��غ�ˮ�����Ե�صķ�Ӧ�����ӷ���ʽΪ��CH4+2O2+2OH-=CO32-+3H2O����������������������Һ��PH��С�������������������õ����ӷ�����ԭ��Ӧ���缫��ӦʽΪ��O2+2H2O+4e-=4OH-������ܷ�Ӧ�����ӷ���ʽ��ȥ�����缫��Ӧ��2���õ������缫��Ӧ��CH4+10OH--8e-=CO32-+7H2O��
�ʴ�Ϊ��CH4+10OH--8e-=CO32-+7H2O��CH4+2O2+2OH-=CO32-+3H2O����С��
���� ���⿼����ԭ��صĹ���ԭ����Ӧ�ã��缫���ƣ��缫�жϣ��缫��Ӧ����ط�Ӧ����������ԭ��صĻ���֪ʶ�����廯�ϼ۱仯�ж�������Ӧ����ԭ��Ӧ�������غ��ǽ���ؼ���

 ��У����ϵ�д�
��У����ϵ�д���1����������������Ӧ����1molˮ��������241.8kJ��д���÷�Ӧ���Ȼ�ѧ����ʽH2��g��+$\frac{1}{2}$O2��g��=H2O��g����H=-241.8kJ/mol����1gˮ����ת����Һ̬ˮ����2.444kJ����Ӧ2H2��g��+O2��g���T2H2O��l���ġ�H=-571.6kJ/mol��������ȼ����Ϊ285.8kJ/mol��
��2������̬��̬ԭ���γ�1mol��ѧ���ͷŵ���������м��ܣ��ӻ�ѧ���ĽǶȷ�������ѧ��Ӧ�Ĺ��̾��Ƿ�Ӧ��Ļ�ѧ�����ƻ���������Ļ�ѧ�����γɹ��̣��ڻ�ѧ��Ӧ�����У��ƻ��ɻ�ѧ����Ҫ�����������γ��»�ѧ���ֻ��ͷ�������
| ��ѧ�� | H-H | N-H | N��N |
| ����/kJ•mol-1 | 436 | 391 | 945 |
��3�����ݸ�˹���ɿ��Զ�ijЩ����ͨ��ʵ��ֱ�Ӳⶨ�Ļ�ѧ��Ӧ���ʱ�������㣮
��֪��C��s��ʯī��+O2��g���TCO2��g����H1=-393.5kJ•mol-1
2H2��g��+O2��g���T2H2O��l����H2=-571.6kJ•mol-1
2C2H2��g��+5O2��g���T4CO2��g��+2H2O��l����H3=-2 599kJ•mol-1
���ݸ�˹���ɣ�����298Kʱ��C��s��ʯī����H2��g������1mol C2H2��g����Ӧ���ʱ䣨�г��ļ���ʽ������H=2��H1+$\frac{1}{2}$��H2-$\frac{1}{2}$��H3=+226.7kJ•mol-1��
| A�� |  ��ҩʹ�� ��ҩʹ�� | B�� |  ��ʳ��� | C�� |  ת������ | D�� |  ����ұ�� |
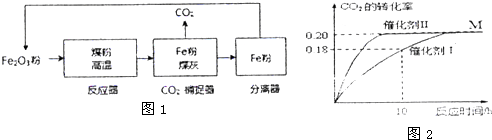
 ��1����ӦFe��s��+CO2��g��?FeO��s��+CO��g����H1��ƽ�ⳣ��ΪK1����ӦFe��s��+H2O��g��?FeO��s��+H2��g����H2��ƽ�ⳣ��ΪK2���ڲ�ͬ�¶�ʱK1��K2��ֵ�����
��1����ӦFe��s��+CO2��g��?FeO��s��+CO��g����H1��ƽ�ⳣ��ΪK1����ӦFe��s��+H2O��g��?FeO��s��+H2��g����H2��ƽ�ⳣ��ΪK2���ڲ�ͬ�¶�ʱK1��K2��ֵ�����| 700�� | 900�� | |
| K1 | 1.47 | 2.15 |
| K2 | 2.38 | 1.67 |
��2��һ���¶��£���ij�ܱ������м����������۲�����һ������CO2���壬������ӦFe��s��+CO2��g��?FeO��s��+CO��g����H��0��CO2��Ũ����ʱ��Ĺ�ϵ��ͼ��ʾ��
�ٸ������·�Ӧ��ƽ�ⳣ��Ϊ2.0��������������CO2����ʼŨ��Ϊ2.0mol•L-1����ƽ��ʱCO2��Ũ��Ϊ$\frac{2}{3}$mol•L-1��
�����д�ʩ����ʹƽ��ʱK�������A����ѡ����ĸ����
A�������¶� B������ѹǿC���ٳ���һ������CO2 D���ټ���һ�������ۣ�
| A�� | ��ȡ��̼���ڼ�����ʽ | |
| B�� | ���չ涨�������������з������ | |
| C�� | �������մ����ո� | |
| D�� | ����ũ���������������֪ʶ |
| A�� | ����ϩ�����к�̼̼˫�� | B�� | ��֬��������Ӧ���ڼӳɷ�Ӧ | ||
| C�� | ������3��ͬ���칹�� | D�� | �Ե���Ϊԭ�Ͽ����Ʊ��Ҵ� |