题目内容
10.按要求准确表达下列变化过程中的化学用语,其中(1)~(3)写化学方程式,(4)~(5)写离子方程式.(1)工业粗硅的制取SiO2+2C$\frac{\underline{\;高温\;}}{\;}$Si+2CO↑
(2)铝片投入氢氧化钠溶液2Al+2H2O+2NaOH═2NaAlO2+3H2↑
(3)写出焊接钢轨的化学方程式2Al+Fe2O3$\frac{\underline{\;高温\;}}{\;}$2Fe+Al2O3
(4)实验室中氢氧化铝的制取Al3++3NH3•H2O═Al(OH)3↓+3NH4+
(5)氧化铝溶于氢氧化钠溶液Al2O3+2OH-═2AlO2-+H2O.
分析 (1)工业上常用碳在高温下与二氧化硅反应制取粗硅;
(2)铝与氢氧化钠溶液反应生成偏铝酸钠和氢气;
(3)铝和铁的氧化物高温反应生成熔融铁和氧化铝;
(4)硫酸铝与氨水反应生成氢氧化铝沉淀和硫酸铵;
(5)氧化铝与氢氧化钠溶液反应生成偏铝酸钠和水.
解答 解:(1)碳在高温下与二氧化硅反应生成硅与一氧化碳,SiO2+2C$\frac{\underline{\;高温\;}}{\;}$Si+2CO↑;
故答案为:SiO2+2C$\frac{\underline{\;高温\;}}{\;}$Si+2CO↑;
(2)铝与氢氧化钠溶液反应生成偏铝酸钠和氢气,化学方程式:2Al+2H2O+2NaOH═2NaAlO2+3H2↑;
故答案为:2Al+2H2O+2NaOH═2NaAlO2+3H2↑;
(3)铝和铁的氧化物高温反应生成熔融铁和氧化铝,化学方程式:2Al+Fe2O3$\frac{\underline{\;高温\;}}{\;}$2Fe+Al2O3,
故答案为:2Al+Fe2O3$\frac{\underline{\;高温\;}}{\;}$2Fe+Al2O3;
(4)硫酸铝与氨水反应生成氢氧化铝沉淀和硫酸铵,离子方程式:Al3++3NH3•H2O═Al(OH)3↓+3NH4+;
故答案为:Al3++3NH3•H2O═Al(OH)3↓+3NH4+;
(5)氧化铝与氢氧化钠溶液反应生成偏铝酸钠和水,离子方程式:Al2O3+2NaOH═2NaAlO2+H2O,
故答案为:Al2O3+2OH-═2AlO2-+H2O;
点评 本题考查了化学方程式、离子方程式的书写,明确反应实质是解题关键,题目难度不大.

练习册系列答案
 文敬图书课时先锋系列答案
文敬图书课时先锋系列答案
相关题目
6.在元素周期表中,磷元素的某些信息如图所示.下列说法不正确的是( )
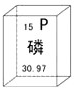

| A. | 磷元素为非金属元素 | B. | 磷原子核外有15个电子 | ||
| C. | 磷的原子序数为15 | D. | 相对原子质量为30.97g |
4.一定条件下,可逆反应X(g)+3Y(g)?2Z(g),若X、Y、Z的起始浓度分别为C1、C2、C3(均不为0),平衡时,X、Y、Z的浓度分别为0.1mol/L、0.3mol/L/、0.08mol/L,下列判断不合理的是( )
| A. | C1:C2=1:3 | B. | 平衡时,X和Z的生成速率之比为1:2 | ||
| C. | X、Y的转化率不相等 | D. | C1的取值范围为0<C1<0.14mol/L |
2.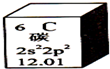 元素周期表是学习化学的重要工具.下图是元素周期表中的一格,以下对该图信息的解读中,不正确的是( )
元素周期表是学习化学的重要工具.下图是元素周期表中的一格,以下对该图信息的解读中,不正确的是( )
 元素周期表是学习化学的重要工具.下图是元素周期表中的一格,以下对该图信息的解读中,不正确的是( )
元素周期表是学习化学的重要工具.下图是元素周期表中的一格,以下对该图信息的解读中,不正确的是( )| A. | 该元素的三种核素质子数均为6 | B. | 该元素原子最外层有4个电子 | ||
| C. | 该元素的相对原子质量为12.01 | D. | 该元素的原子核外有三个电子层 |
19.下列现象与氢键有关的是( )
①NH3的熔、沸点比PH3的高
②乙醇、乙酸可以和水以任意比互溶
③冰的密度比液态水的密度小
④尿素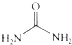 的熔、沸点比醋酸
的熔、沸点比醋酸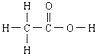 的高.
的高.
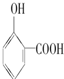
⑤晶体熔点的高低: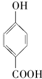 >
>
⑥水分子高温下很稳定.
①NH3的熔、沸点比PH3的高
②乙醇、乙酸可以和水以任意比互溶
③冰的密度比液态水的密度小
④尿素
 的熔、沸点比醋酸
的熔、沸点比醋酸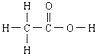 的高.
的高.⑤晶体熔点的高低:
 >
>
⑥水分子高温下很稳定.
| A. | ①②③④⑤⑥ | B. | ①②③④⑤ | C. | ①②③④ | D. | ①②③ |
20.把amolH2和bmolC2H4混合,在一定条件下使他们一部分发生反应生成wmol C2H6,将反应后所得的混合气体完全燃烧,消耗O2的物质的量为( )
| A. | a+3b | B. | $\frac{a}{2}$+3b | C. | $\frac{a}{2}$+3b+$\frac{7w}{2}$ | D. | $\frac{a}{2}$+3b-$\frac{7w}{2}$ |
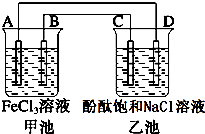 如图所示,甲池中电池反应式为2Fe3++Cu═2Fe2++Cu2+,反应过程中A电极质量逐渐减小,C、D为石墨电极,乙池中为200mL滴加酚酞的饱和NaCl溶液.回答下列问题:
如图所示,甲池中电池反应式为2Fe3++Cu═2Fe2++Cu2+,反应过程中A电极质量逐渐减小,C、D为石墨电极,乙池中为200mL滴加酚酞的饱和NaCl溶液.回答下列问题: