题目内容
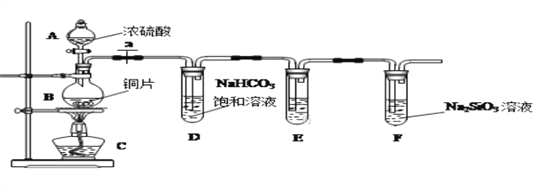
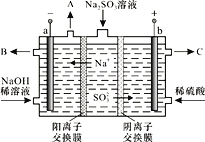
【题目】某科研机构用NaOH溶液吸收硫酸工业废气中的SO2,将所得的Na2SO3溶液进行电解,可循环再生NaOH,同时得到某种副产物,其原理如图所示(电极材料为石墨)。
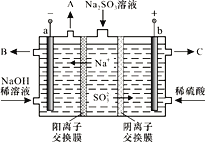
(1)当有1molNa+通过阳离子交换膜时,a极生成气体__________L(标准状况),阳极的电极反应式是______________________________。
(2)稀NaOH溶液的作用是____________,B处流出较浓的NaOH溶液,C处流出的是________________。
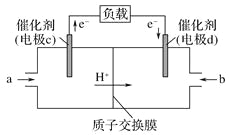
(3)在标准状况下,若用甲烷-空气燃料电池做电源,处理含SO2 20%(体积分数)的废气40m3,理论上需要消耗甲烷___________m3。
【答案】 11.2 SO32- -2e-+H2O==SO42- +2H+ 增强溶液导电性 较浓的硫酸 2
【解析】根据装置图中正负极和溶液中离子的移动方向及放电能力,即可判断出两极产物,进而写出电极反应式;由于水中离子浓度很小,所以稀NaOH溶液和稀硫酸的作用都是增强溶液的导电性;根据电子转移守恒,可计算出消耗甲烷的体积。
(1) 当有1mol Na+通过阳离子交换膜时,即电路中通过1mol电子,在阴极放出H2在标准状况下的体积为11.2L;而在阳极上SO32-放电生成SO42-,电极反应式为SO32--2e-+H2O==SO42-+2H+。
(2)由于水中离子浓度很小,所以用稀NaOH溶液和稀硫酸增强溶液的导电性,提高工作效率;根据阳极反应式可知,从C处流出的物质是较浓的硫酸。
(3)处理含SO2 20%(体积分数)的废气40m3,则n(SO2)=[40×103L×20%]/22.4L/mol= 8000/22.4mol,则转移电子n(e-)=8000/11.2mol,而1molCH4在燃料电池中反应生成1mol CO2转移8mol电子,所以理论上需要消耗甲烷的体积为![]() ×10-3m3/L =2 m3。
×10-3m3/L =2 m3。

 周周清检测系列答案
周周清检测系列答案 轻巧夺冠周测月考直通高考系列答案
轻巧夺冠周测月考直通高考系列答案【题目】下列离子方程式的书写及评价均合理的是( )
选项 | 离子方程式 | 评价 |
A | 将2 mol Cl2通入含1 mol FeI2的溶液中: 2Fe2++2I-+2Cl2===2Fe3++4Cl-+I2 | 正确;Cl2过量,可将Fe2+、I-均氧化 |
B | Ba(HCO3)2溶液与足量的NaOH溶液反应: Ba2++HCO3-+OH-===BaCO3↓+H2O | 正确;酸式盐与碱反应生成正盐和水 |
C | 过量SO2通入NaClO溶液中: SO2+H2O+ClO-===HClO+HSO3- | 正确;说明酸性:H2SO3强于HClO |
D | 1 mol/L的NaAlO2溶液和2.5 mol/L的HCl溶液等体积混合: 2AlO2-+5H+===Al3++Al(OH)3↓+H2O | 正确;第一步反应和第二步反应消耗的H+的物质的量之比为2∶3 |
A. A B. B C. C D. D
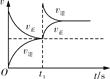
【题目】臭氧在烟气脱硝中的反应为2NO2(g)+O3(g)![]() N2O5(g)+O2(g)。若此反应在恒容密闭容器中进行,下列选项中有关图象对应的分析正确的是( )
N2O5(g)+O2(g)。若此反应在恒容密闭容器中进行,下列选项中有关图象对应的分析正确的是( )
A | B | C | D |
|
|
|
|
平衡后升温,NO2含量降低 | 0~2 s内,v(O3)=0.2 mol·L-1·s-1 | v正:b点>a点 b点:v逆>v正 | 恒温,t1时再充入O3 |
A. AB. BC. CD. D