题目内容
【题目】某研究性学习小组设计了一组实验验证元素周期律。
Ⅰ.甲同学在a、b、c、d四只烧杯中分别加入50 mL冷水,再各滴加几滴酚酞试液,依次加入大小相近的钠(Na)、镁(Mg)、铝(Al)、钾(K)金属块,观察现象。
(1)甲同学设计实验的目的是验证:同一主族,从上到下金属元素的原子失电子能力逐渐增强;同一周期,从左到右金属元素的原子失电子能力逐渐___________________;
(2)反应最剧烈的烧杯中金属是_______(填字母序号);
A.钠 B.镁 C.铝 D.钾
(3)实验中发现b、c两只烧杯中几乎没有什么现象,要想达到实验目的,请你帮助选择下列合适的方法_________(填字母序号)。
A.把镁、铝的金属块换成金属粉末
B.把烧杯中的冷水换成热水
C.把烧杯中的冷水换成盐酸
D.把烧杯中的冷水换成氢氧化钠溶液
Ⅱ.乙同学设计实验探究碳、硅元素的非金属性的相对强弱。根据要求完成下列各题
(1)实验装置:

(1)填写所示仪器名称:B__________
(2)实验步骤:
连接仪器、_____________、加药品后,打开 a、然后滴入浓硫酸,加热
(3)问题探究:(已知酸性强弱:亚硫酸 >碳酸)
①铜与浓硫酸反应的化学方程式是________________________________;装置E中酸性KMnO4溶液的作用是_____________________________;
②能说明碳元素的非金属性比硅元素非金属性强的实验现象是__________________;试管F中发生反应的离子方程式为_____________________。
③依据试管 D 中的反应,能否证明S的非金属性强于C的非金属性___(填 “能”或“否”)。
【答案】 减弱 D BC 圆底烧瓶 检查装置的气密性 Cu+2H2SO4(浓) ![]() CuSO4 +SO2↑+2H2O 吸收SO2 E试管中的溶液褪色不完全,F试管中出现白色沉淀 CO2+H2O+SiO32- =H2SiO3↓+CO32- 或 2CO2+2H2O+SiO32- =H2SiO3↓+2HCO3- 否
CuSO4 +SO2↑+2H2O 吸收SO2 E试管中的溶液褪色不完全,F试管中出现白色沉淀 CO2+H2O+SiO32- =H2SiO3↓+CO32- 或 2CO2+2H2O+SiO32- =H2SiO3↓+2HCO3- 否
【解析】Ⅰ.(1)同一周期,从左到右,原子失电子能力减弱,则元素金属性逐渐减弱,故答案为:减弱;
(2)金属性K>Na>Mg>Al,金属性越强,单质与水反应越剧烈,故反应最剧烈的烧杯是D,故答案为:D;
(3)反应现象不明显,是因为镁和铝常温下与水几乎不反应。A.把镁、铝的金属块换成金属粉末,现象应该仍不明显,错误;B.把烧杯中的冷水换成热水,升高温度可以加快速率,镁会看到明显的现象,正确;C.把烧杯中的冷水换成盐酸,增大了溶液中氢离子的浓度,可以加快速率,会看到明显的现象的差别,正确;D.不能通过金属与碱反应的难易程度判断金属性的强弱,错误;故答案为:BC;
Ⅱ.(1)B名称是圆底烧瓶,故答案为:圆底烧瓶;
(2)连接好仪器后,要检验装置气密性,然后装药品,否则易导致实验失败,故答案为:检验装置气密性;
(3)①铜和浓硫酸在加热条件下发生反应生成硫酸铜、二氧化硫和水,反应方程式为Cu+2H2SO4(浓)![]() CuSO4+SO2↑+2H2O;二氧化硫具有还原性,能被酸性高锰酸钾溶液氧化,所以可以用酸性高锰酸钾溶液除去二氧化硫气体,故答案为:Cu+2H2SO4(浓)
CuSO4+SO2↑+2H2O;二氧化硫具有还原性,能被酸性高锰酸钾溶液氧化,所以可以用酸性高锰酸钾溶液除去二氧化硫气体,故答案为:Cu+2H2SO4(浓)![]() CuSO4+SO2↑+2H2O;除去二氧化硫气体;
CuSO4+SO2↑+2H2O;除去二氧化硫气体;
②E试管中的溶液褪色不完全,说明气体中没有二氧化硫,F试管中出现白色沉淀说明二氧化碳与硅酸钠反应生成了硅酸沉淀,说明碳元素的非金属性比硅元素非金属性强;反应的离子方程式为CO2+SiO32-+H2O=H2SiO3↓+CO32-,故答案为:E试管中的溶液褪色不完全,F试管中出现白色沉淀;CO2+SiO32-+H2O=H2SiO3↓+CO32-;
③元素的非金属性越强,其最高价氧化物的水化物酸性越强,不能根据其非最高价氧化物的水化物酸性强弱判断非金属性强弱,亚硫酸不是S元素的最高价氧化物的水化物,所以不能据此判断非金属性强弱,故答案为:否。

【题目】实验室制备1,2﹣二溴乙烷的反应原理如下:
CH3CH2OH ![]() CH2═CH2
CH2═CH2
CH2═CH2+Br2→BrCH2CH2Br
可能存在的主要副反应有:乙醇在浓硫酸的存在下在l40℃脱水生成乙醚.用少量的溴和足量的乙醇制备1,2﹣二溴乙烷的装置如图所示:
有关数据列表如下:
乙醇 | 1,2﹣二溴乙烷 | 乙醚 | |
状态 | 无色液体 | 无色液体 | 无色液体 |
密度/gcm﹣3 | 0.79 | 2.2 | 0.71 |
沸点/℃ | 78.5 | 132 | 34.6 |
熔点/℃ | 一l30 | 9 | ﹣1l6 |
回答下列问题: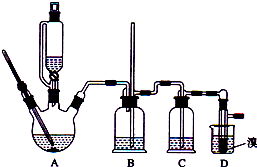
(1)在此制各实验中,要尽可能迅速地把反应温度提高到170℃左右,其最主要目的是;(填正确选项前的字母)
a.引发反应 b.加快反应速度 c.防止乙醇挥发 d.减少副产物乙醚生成
(2)在装置C中应加入 , 其目的是吸收反应中可能生成的酸性气体:(填正确选项前的字母)
a.水 b.浓硫酸 c.氢氧化钠溶液 d.饱和碳酸氢钠溶液
(3)判断该制备反应已经结束的最简单方法是;
(4)将1,2﹣二溴乙烷粗产品置于分液漏斗中加水,振荡后静置,产物应在层(填“上”、“下”);
(5)若产物中有少量未反应的Br2 , 最好用洗涤除去;(填正确选项前的字母)
a.水 b.氢氧化钠溶液 c.碘化钠溶液 d.乙醇
(6)若产物中有少量副产物乙醚.可用的方法除去;
(7)反应过程中应用冷水冷却装置D,其主要目的是;但又不能过度冷却(如用冰水),其原因是 .

