题目内容
15.在实验室里可用如图1所示装置制取氯酸钾、次氯酸钠和探究氯水的性质.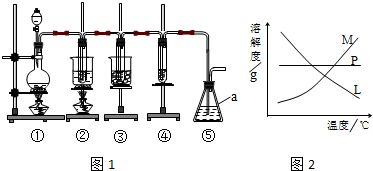
图1中:①为氯气发生装置;②的试管里盛有15mL 30% KOH溶液,并置于水浴中;③的试管里盛有15mL 8% NaOH溶液,并置于冰水浴中;④的试管里盛有紫色石蕊溶液.
请回答下列问题:
(1)仪器a的名称是锥形瓶.
(2)实验室制取氯气的离子方程式为MnO2+4H++2Cl-$\frac{\underline{\;\;△\;\;}}{\;}$Mn2++Cl2↑+2H2O.为了除去氯气中的氯化氢气体,可在①与②之间安装盛有B(填字母代号)的净化装置.
A.碱石灰B.饱和食盐水C.浓硫酸D.饱和碳酸氢钠溶液
(3)比较制取氯酸钾和次氯酸钠的条件,二者的差异是制取温度不同、制取时碱的浓度也不同.反应完毕经冷却后,②的试管中有大量晶体析出.在图2中符合该晶体溶解度曲线的是M(填字母代号);从②的试管中分离出晶体的操作是过滤,该操作需要用到的玻璃仪器有普通漏斗、玻璃棒、烧杯.
(4)次氯酸钠中存在的化学键类型为离子键、共价键.
(5)实验中可观察到④的试管里溶液的颜色发生了如下变化,请完成下表中的空白:
| 实验现象 | 原因 |
| 溶液最初从紫色逐渐变为红色 | 氯气与水反应生成的H+使石蕊变色 |
| 随后溶液逐渐变为无色 | 氯气与水反应生成的HClO将石蕊氧化为无色物质 |
| 然后溶液从无色逐渐变为浅黄绿色色 | 继续通入的氯气溶于水使溶液呈浅黄绿色 |
分析 (1)根据仪器a的构造写出其名称;
(2)实验室中用浓盐酸与二氧化锰加热反应制取氯气,据此写出反应的离子方程式;可用饱和食盐水除去氯气中的氯化氢气体;
(3)由题目信息可知,在加热条件下,氯气与浓KOH溶液反应生成氯酸钾,在常温以下,氯气与稀NaOH溶液反应生成次氯酸钠;②的试管中有大量晶体析出,说明溶质的溶解度随温度的降低而降低,据此进行判断;分离固体与液体通常采用过滤的方法;根据过滤操作方法写出其使用的仪器名称;
(4)次氯酸钠为离子化合物,次氯酸钠中既存在离子键,也存在共价键;
(5)氯气与水反应生成盐酸和次氯酸,反应生成的H+使石蕊变成红色,次氯酸具有强氧化性,将石蕊氧化为无色物质;氯气溶于水后呈浅黄绿色;
(6)有毒气体不能直接排放,需要使用尾气吸收装置.
解答 解:(1)根据仪器a的构造可知,仪器a为锥形瓶,故答案为:锥形瓶;
(2)实验室制取氯气的离子方程式为:MnO2+4H++2Cl-$\frac{\underline{\;\;△\;\;}}{\;}$Mn2++Cl2↑+2H2O;用饱和食盐水除去氯气中的氯化氢气体,故在①与②之间安装盛有饱和食盐水的洗气瓶,所以B正确,
故答案为:MnO2+4H++2Cl-$\frac{\underline{\;\;△\;\;}}{\;}$Mn2++Cl2↑+2H2O;B;
(3)根据题中信息可知,在加热条件下,氯气与浓KOH溶液反应生成氯酸钾,在常温以下,氯气与稀NaOH溶液反应生成次氯酸钠,二者反应的浓度和温度都不相同;
反应完毕经冷却后,②的试管中有大量晶体析出,说明溶质的溶解度随温度的降低而降低,只有M符合;
不溶性固体与液体的分离常采用过滤的方法,过滤操作用到的仪器有:普通漏斗、玻璃棒、烧杯,
故答案为:制取温度不同、制取时碱的浓度也不同;M;过滤;普通漏斗、玻璃棒、烧杯;
(4)次氯酸钠为离子化合物,一定存在离子键,次氯酸还存在氯元素和氧元素形成的共价键,
故答案为:离子键、共价键;
(5)氯气与水反应生成盐酸和次氯酸,反应生成的H+使石蕊变成红色;氯气与水反应生成的HClO,次氯酸具有强氧化性,将石蕊氧化为无色物质;多余的氯气溶于水,使溶液呈浅黄绿色,
故答案为:
| 红 | |
| 氯气与水反应生成的HClO将石蕊氧化为无色物质 | |
| 浅黄绿 | 继续通入的氯气溶于水使溶液呈浅黄绿色 |
点评 本题考查对装置的分析评价、物质的分离提纯、对实验现象的分析等知识点,试题难度中等,该类试题综合性强,难易适中,有利于培养学生的逻辑推理能力和规范严谨的实验设计能力;该类试题主要是以常见仪器的选用、实验基本操作为中心,重点考查实验基本操作的规范性和准确及灵活运用知识解决实际问题的能力.

 寒假乐园北京教育出版社系列答案
寒假乐园北京教育出版社系列答案| A. | 单质的密度依次增大 | B. | 单质的熔点和沸点依次升高 | ||
| C. | Cl2可以从KI溶液中置换出I2 | D. | Br2可以从NaCl溶液中置换出Cl2 |
| A. | 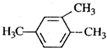 1,3,4-三甲基苯 1,3,4-三甲基苯 | B. | 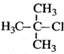 2-甲基-1-氯丙烷 2-甲基-1-氯丙烷 | ||
| C. | 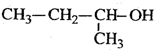 2-甲基-1-丙醇 2-甲基-1-丙醇 | D. | 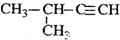 2-甲基-3-丁炔 2-甲基-3-丁炔 |
| A. | ①② | B. | ①③ | C. | ④ | D. | 均不正确 |
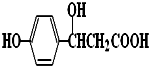 它可以发生的反应类型有:( )
它可以发生的反应类型有:( )(a)取代 (b)加成 (c)消去 (d)酯化 (e)水解 (f)中和 (g)缩聚 (h)加聚.
| A. | (a)(c)(d)(f) | B. | (b)(e)(f)(h) | C. | (a)(b)(c)(d) | D. | 除(e)(h)外 |
| A. | 0.1mol乙炔分子中含有的共用电子对数目为0.5NA | |
| B. | 常温常压,1.6g甲烷含有的质子数为NA | |
| C. | 14g乙烯和环丙烷混合物中含有的碳原子数目为NA | |
| D. | 在标准状态下,2.24L己烷含有的氢原子数目为1.4NA |
| A. | A原子的N层电子数比B原子的N层电子数一定少 | |
| B. | A原子的外围电子数比B原子的外围电子数可能多 | |
| C. | A元素一定是副族元素,B元素可能是副族元素,也可能是主族元素 | |
| D. | A元素一定是副族元素,B元素一定是主族元素 |
| A. | 酒精与水-蒸馏 | B. | 油与水-分液 | C. | 食盐与水-蒸发 | D. | KNO3与NaCl-过滤 |