题目内容
7.已知位于第4周期的A、B两元素,A原子的M层电子数比B原子的M层电子数少7个.下列说法正确的是( )| A. | A原子的N层电子数比B原子的N层电子数一定少 | |
| B. | A原子的外围电子数比B原子的外围电子数可能多 | |
| C. | A元素一定是副族元素,B元素可能是副族元素,也可能是主族元素 | |
| D. | A元素一定是副族元素,B元素一定是主族元素 |
分析 A、如第4周期21号的Sc和28号的Ni,满足A原子的M层电子数比B原子的M层电子数少7个,但N层电子数相等;
B、如23号的V和31号的Ga,满足A原子的M层电子数比B原子的M层电子数少7个,但V的外围电子数为电子排布为3d34s2,而Ga的外围电子排布为:4s24p1;
C、如第4周期21号的Sc和28号的Ni、23号的V和31号的Ga,都满足A原子的M层电子数比B原子的M层电子数少7个;
D、如第4周期21号的Sc和28号的Ni、23号的V和31号的Ga,都满足A原子的M层电子数比B原子的M层电子数少7个.
解答 解:A、如第4周期21号的Sc和28号的Ni,满足A原子的M层电子数比B原子的M层电子数少7个,但N层电子数相等,而不是A原子的N层电子数比B原子的N层电子数一定少,故A错误;
B、如23号的V和31号的Ga,满足A原子的M层电子数比B原子的M层电子数少7个,但V的外围电子数为电子排布为3d34s2,外围电子数为5,而Ga的外围电子排布为:4s24p1,外围电子数为3,所以A原子的外围电子数比B原子的外围电子数可能多,故B正确;
C、如第4周期20号的Ca和27号的Co,满足A原子的M层电子数比B原子的M层电子数少7个,所以A元素不一定是副族元素,B元素可能是副族元素 也可能是主族元索,故C错误;
D、23号的V和31号的Ga,都满足A原子的M层电子数比B原子的M层电子数少7个,Ga是主族元素,故D错误;
故选B.
点评 本题考查原子结构与元素周期表的关系,为高频考点,答题时要逐步确定A、B的电子层数和各层上的电子数,把排布规律与题意结合起来,整体把握,难度不大.

练习册系列答案
相关题目
17.下列说法正确的是( )
| A. | 若把H2S写成H3S,则违背了共价键的饱和性 | |
| B. | H3O+的存在说明共价键不应有饱和性 | |
| C. | 所有共价键都有方向性 | |
| D. | 两原子轨道发生重叠后,电子在两核间出现的概率减小 |
18.下列说法正确的是( )
①煤经气化和液化两个化学变化过程,可变为清洁能源
②甲烷、乙烯和苯在工业上都可通过石油分馏得到
③食用白糖的主要成分是蔗糖
④用饱和食盐水替代水跟电石作用,可以有效控制产生乙炔的速率
⑤乙烯、氯乙烯、聚乙烯均可使酸性高锰酸钾溶液褪色
⑥纤维素、合成纤维、光导纤维都是有机高分子化合物
⑦制肥皂时,在皂化液里加入饱和食盐水,能够促进高级脂肪酸钠的析出
⑧苯酚稀溶液常用于外科消毒,所以自来水也可以用苯酚进行消毒处理
⑨重结晶法提纯苯甲酸时,为除去杂质和防止苯甲酸析出,应该趁热过滤.
①煤经气化和液化两个化学变化过程,可变为清洁能源
②甲烷、乙烯和苯在工业上都可通过石油分馏得到
③食用白糖的主要成分是蔗糖
④用饱和食盐水替代水跟电石作用,可以有效控制产生乙炔的速率
⑤乙烯、氯乙烯、聚乙烯均可使酸性高锰酸钾溶液褪色
⑥纤维素、合成纤维、光导纤维都是有机高分子化合物
⑦制肥皂时,在皂化液里加入饱和食盐水,能够促进高级脂肪酸钠的析出
⑧苯酚稀溶液常用于外科消毒,所以自来水也可以用苯酚进行消毒处理
⑨重结晶法提纯苯甲酸时,为除去杂质和防止苯甲酸析出,应该趁热过滤.
| A. | ②④⑤⑦⑧ | B. | ①③④⑦⑨ | C. | ①⑤⑥⑧⑨ | D. | ①②③⑤⑥ |
15.在实验室里可用如图1所示装置制取氯酸钾、次氯酸钠和探究氯水的性质.
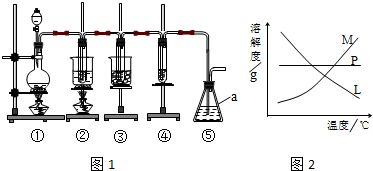
图1中:①为氯气发生装置;②的试管里盛有15mL 30% KOH溶液,并置于水浴中;③的试管里盛有15mL 8% NaOH溶液,并置于冰水浴中;④的试管里盛有紫色石蕊溶液.
请回答下列问题:
(1)仪器a的名称是锥形瓶.
(2)实验室制取氯气的离子方程式为MnO2+4H++2Cl-$\frac{\underline{\;\;△\;\;}}{\;}$Mn2++Cl2↑+2H2O.为了除去氯气中的氯化氢气体,可在①与②之间安装盛有B(填字母代号)的净化装置.
A.碱石灰B.饱和食盐水C.浓硫酸D.饱和碳酸氢钠溶液
(3)比较制取氯酸钾和次氯酸钠的条件,二者的差异是制取温度不同、制取时碱的浓度也不同.反应完毕经冷却后,②的试管中有大量晶体析出.在图2中符合该晶体溶解度曲线的是M(填字母代号);从②的试管中分离出晶体的操作是过滤,该操作需要用到的玻璃仪器有普通漏斗、玻璃棒、烧杯.
(4)次氯酸钠中存在的化学键类型为离子键、共价键.
(5)实验中可观察到④的试管里溶液的颜色发生了如下变化,请完成下表中的空白:
(6)装置⑤的作用是吸收尾气,防止污染.

图1中:①为氯气发生装置;②的试管里盛有15mL 30% KOH溶液,并置于水浴中;③的试管里盛有15mL 8% NaOH溶液,并置于冰水浴中;④的试管里盛有紫色石蕊溶液.
请回答下列问题:
(1)仪器a的名称是锥形瓶.
(2)实验室制取氯气的离子方程式为MnO2+4H++2Cl-$\frac{\underline{\;\;△\;\;}}{\;}$Mn2++Cl2↑+2H2O.为了除去氯气中的氯化氢气体,可在①与②之间安装盛有B(填字母代号)的净化装置.
A.碱石灰B.饱和食盐水C.浓硫酸D.饱和碳酸氢钠溶液
(3)比较制取氯酸钾和次氯酸钠的条件,二者的差异是制取温度不同、制取时碱的浓度也不同.反应完毕经冷却后,②的试管中有大量晶体析出.在图2中符合该晶体溶解度曲线的是M(填字母代号);从②的试管中分离出晶体的操作是过滤,该操作需要用到的玻璃仪器有普通漏斗、玻璃棒、烧杯.
(4)次氯酸钠中存在的化学键类型为离子键、共价键.
(5)实验中可观察到④的试管里溶液的颜色发生了如下变化,请完成下表中的空白:
| 实验现象 | 原因 |
| 溶液最初从紫色逐渐变为红色 | 氯气与水反应生成的H+使石蕊变色 |
| 随后溶液逐渐变为无色 | 氯气与水反应生成的HClO将石蕊氧化为无色物质 |
| 然后溶液从无色逐渐变为浅黄绿色色 | 继续通入的氯气溶于水使溶液呈浅黄绿色 |
2.提纯下列物质所选试剂及对应分离方法均可行的是( )
| 物质 | 杂质 | 所选试剂 | 方法 | |
| A | 乙烷 | 乙烯 | 酸性KMnO4溶液 | 洗气 |
| B | 溴苯 | 溴 | H2O | 萃取 |
| C | 乙炔 | 硫化氢 | 硫酸铜溶液 | 洗气 |
| D | 乙酸乙酯 | 乙酸 | 饱和Na2CO3溶液 | 分液 |
| A. | A | B. | B | C. | C | D. | D |
12.下列说法不正确的是( )
| A. | CH3-CH=CH2和CH2=CH2的最简式相同 | |
| B. | CH≡CH和C6H6含碳量相同 | |
| C. | 乙炔和苯互为同系物 | |
| D. | 正戊烷、异戊烷、新戊烷的沸点逐渐降低 |
19.均不属于大气污染物的一组气体是( )
| A. | N2和O2 | B. | CO和CO2 | C. | NO和NO2 | D. | SO2和碳氢化合物 |
16.Murad等三位教授最早提出NO分子在人体内有独特功能,近年来此领域研究有很大进展,因此这三位教授荣获1998年诺贝尔医学及生理学奖.关于NO的下列叙述中不正确的是( )
| A. | NO可以是某些含低价N物质氧化的产物 | |
| B. | NO难溶于水 | |
| C. | NO可以是某些含高价N物质还原的产物 | |
| D. | NO是红棕色气体 |
17.下列物质既能与金属钠作用放出气体,又能与纯碱作用放出气体的是( )
| A. | C2H5OH | B. | H2O | C. | CH3COOH | D. | C6H12 |