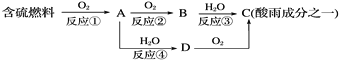МвДїДЪИЭ
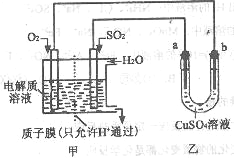
ЎѕМвДїЎїОЄБЛМЅѕїCl2ЎўSO2Н¬К±НЁИлH2OЦР·ўЙъµД·ґУ¦Ј¬ДіРЈ»ЇС§РЛИ¤РЎЧйН¬С§ЙијЖБЛИзНјЛщКѕµДКµСйЧ°ЦГЎЈ

ЈЁ1Ј©ёГ»ЇС§РЛИ¤РЎЧйµДН¬С§ОЄЦЖИЎCl2ЎўSO2ЖшМеЈ¬ПЦІЙУГNa2SO3Ул70%µДБтЛбОЄФБПЦЖИЎSO2Ј¬ІЙУГMnO2єНЕЁСОЛб(12 molЎ¤LЈ1)ОЄФБПЦЖИЎCl2ЎЈФЪґЛКµСйЦРЈ¬FТЗЖчµДЧчУГКЗ________Ј»·ўЙъЧ°ЦГBУ¦СЎФсТФПВИэЦЦЧ°ЦГЦРµД________(МоРтєЕ)ЎЈ

ЈЁ2Ј©DЧ°ЦГЦРЦчТЄ·ґУ¦µДАлЧУ·ЅіМКЅОЄ____________________________________________________ЎЈ
ЈЁ3Ј©ОЄСйЦ¤НЁИлDЧ°ЦГЦРµДЖшМеКЗCl2№эБї»№КЗSO2№эБїЈ¬РЛИ¤РЎЧйµДН¬С§Чј±ёБЛТФПВКФјБЈє
ўЩВИ»ЇМъИЬТєЎЎўЪВИ»ЇСЗМъИЬТєЎЎўЫБтЗи»ЇјШИЬТєЎЎўЬЛбРФёЯГМЛбјШИЬТє
ИфCl2№эБїЈ¬ИЎККБїDЦРИЬТєµОјУЦБКўУР________(МоТ»ёцРтєЕЈ¬ПВН¬)КФјБµДКФ№ЬДЪЈ¬ФЩјУИл________КФјБЎЈ·ўЙъµДПЦПуКЗ_____________________________________________ЎЈ
ИфSO2№эБїЈ¬ИЎККБїDЦРИЬТєµОјУЦБКўУР________КФјБµДКФ№ЬДЪЈ¬·ўЙъµДПЦПуКЗ________________________________________________________________________ЎЈ
Ўѕґр°ёЎї ·Аµ№Оь ўЩ Cl2Ј«SO2Ј«2H2OЈЅ4HЈ«Ј«SO42ЈЈ«2ClЈ ўЪ ўЫ ИЬТєіКємЙ« ўЬ ЧПємЙ«НКОЄОЮЙ«
ЎѕЅвОцЎїЈЁ1Ј©SO2ТЧУлЛ®·ґУ¦Ј¬ЗТИЬЅв¶ИЅПґу»б·ўЙъµ№ОьЈ¬ФтFЧ°ЦГµДЧчУГКЗїЙТФ·Аµ№ОьЈ¬Ч°ЦГBОЄЦЖИЎВИЖшµДЧ°ЦГЈ¬УЙ№МТє·ґУ¦ЗТјУИИµДФАнїЙЦЄУ¦СЎФсўЩЈ»ЈЁ2Ј©DЦРКЗ¶юСх»ЇБтєНВИЖш·ўЙъµДСх»Ї»№Ф·ґУ¦ЙъіЙБтЛбєНСОЛбЈ¬·ґУ¦µДАлЧУ·ЅіМКЅОЄCl2Ј«SO2Ј«2H2OЈЅ4HЈ«Ј«SO42ЈЈ«2ClЈЈ»ЈЁ3Ј©ИфCl2№эБїЈ¬ВИЛ®ѕЯУРЗїСх»ЇРФЈ¬ФтїЙТФИЎККБїDЦРИЬТєµОјУЦБКўУРВИ»ЇСЗМъИЬТєКФјБµДКФ№ЬДЪЈ¬ФЩјУИлБтЗи»ЇјШИЬТє»б±дСЄємЙ«Ј¬Ц¤ГчВИЖшСх»ЇСЗМъАлЧУЈ»ИфSO2№эБїЈ¬¶юСх»ЇБтѕЯУР»№ФРФЈ¬ФтїЙТФИЎККБїDЦРИЬТєµОјУЦБКўУРЛбРФёЯГМЛбјШИЬТєµДКФ№ЬЦРЈ¬¶юСх»ЇБт±»Сх»ЇЈ¬ТтґЛЧПємЙ«НКОЄОЮЙ«Ц¤Гчє¬УР¶юСх»ЇБтЎЈ

ЎѕМвДїЎїНкіЙПВБРёчМвЈ®
(1)іЈОВПВЈ¬ЕЁ¶ИѕщОЄ 0.1molL©Ѓ1 µДПВБРОеЦЦДЖСОИЬТєµД pH Из±нЈ»
ИЬЦК | CH3COONa | NaHCO3 | Na2CO3 | NaClO | NaCN |
pH | 8.8 | 9.7 | 11.6 | 10.3 | 11.1 |
ЙПКцСОИЬТєЦРµДТхАлЧУЈ¬ЅбєПH+ДЬБ¦ЧоЗїµДКЗ Ј¬ёщѕЭ±нЦРКэѕЭЈ¬ЕЁ¶ИѕщОЄ0.01molL©Ѓ1 µДПВБРЛДЦЦЛбµДИЬТє·Ц±рПЎКН 100±¶Ј¬pH±д»ЇЧоґуµДКЗ (Мо±аєЕ)Ј®
AЈ®HCN BЈ®HClO CЈ®CH3COOH DЈ®H2CO3
(2)УРўЩ100ml 0.1mol/L NaHCO3ўЪ100ml 0.1mol/L Na2CO3 БЅЦЦИЬТєЈє
ИЬТєЦРЛ®µзАліцµДOH-ёцКэЈєўЩ ўЪ(МоЎ°ЈѕЎ±ЎўЎ°=Ў±»тЎ°ЈјЎ±Ј¬ПВН¬)Ј®
ИЬТєЦРТхАлЧУµДОпЦКµДБїЕЁ¶ИЦ®єНЈєўЩ ўЪЈ®
(3)NaCNУцЛ®їЙІъЙъТЧИјµДHCNЖшМеЈ¬ЕЁ¶ИѕщОЄ0.1molЈЇLµДNaCNєНHCNµД»мєПТєЦРµОјУ·УМЄЈ¬ИЬТє±дємЈ¬Фт»мєПТєЦРёчАлЧУµДЕЁ¶ИґуРЎ№ШПµОЄ_______________________ЎЈ
(4)СРѕїЦ¤КµЈ¬CO2їЙФЪЛбРФЛ®ИЬТєЦРНЁ№эµзЅвЙъіЙјЧґј(CH3OH)Ј¬ФтЙъіЙјЧґјµД·ґУ¦·ўЙъФЪ (МоТхј«»тСфј«)Ј¬ёГµзј«·ґУ¦КЅКЗ ЎЈ
(5)ТСЦЄKsp(CuS)ЈЅ1.3ЎБ10Ј36Ј¬Ksp(NiS)ЈЅ1.0ЎБ10Ј24Ј»ФЪє¬Cu2Ј«Ј¬Ni2Ј«µДИЬТєЦРЈ¬µ±Ni2Ј«ЗЎєГНкИ«іБµн[ґЛК±ИЬТєЦРc(Ni2Ј«)ЈЅ1.0ЎБ10Ј5 molЎ¤LЈ1]Ј¬ИЬТєЦРCu2Ј«µДЕЁ¶ИКЗ_____________molЎ¤LЈ1ЎЈ