题目内容
9.36克水的物质的量是2mol,它所含氢原子为4mol,含质子数为1.204×1025个.分析 根据n=$\frac{m}{M}$计算水的物质的量,氢原子物质的量为水的2倍,质子物质的量为水的10倍,再根据N=nNA计算质子数目.
解答 解:36g水的物质的量为$\frac{36g}{18g/mol}$=2mol,氢原子物质的量为2mol×2=4mol,含有质子数目为2mol×10×6.02×1023mol-1=1.204×1025,
故答案为:2;4;1.204×1025.
点评 本题考查物质的量有关计算,比较基础,旨在考查学生对基础知识的理解掌握.

练习册系列答案
相关题目
19.下列说法不正确的是( )
| A. | 氯水中加少量的Na2 CO3粉末,可提高溶液中HC1O的浓度 | |
| B. | 金属单质都具有一定的还原性,金属阳离子都只有氧化性 | |
| C. | 火灾现场自救方法是用湿毛巾捂住口鼻并向地势低的地方撤离 | |
| D. | 大气中的N2可作为制硝酸的原料 |
20.下列关于化学用语的表示正确的是( )
| A. | 过氧化钠的电子式:Na${\;}_{•}^{•}$$\underset{\stackrel{••}{O}}{••}$${\;}_{•}^{•}$$\underset{\stackrel{••}{O}}{••}$${\;}_{•}^{•}$Na | |
| B. | 质子数为35、中子数为45的溴原子:${\;}_{35}^{80}$Br | |
| C. | 硫离子的结构示意图: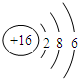 | |
| D. | 间二甲苯的结构简式: |
4.等体积、等浓度的浓硫酸分别与足量的炭粉、铜粉在一定条件下完全反应.下列指定“物理量”之比不是2:1的是( )
| A. | 转移电子的物质的量 | B. | 产生SO2的物质的量 | ||
| C. | 氧化剂的物质的量 | D. | 生成水的物质的量 |
14.下列根据实验操作和实验现象所得出的结论一定正确的是( )
| 选项 | 实验操作 | 实验现象 | 结论 |
| A | 将蘸有浓氨水的玻璃棒靠近溶液X | 有白烟产生 | 溶液X是浓盐酸 |
| B | 用玻璃杯蘸取溶液Y进行焰色反应 | 火焰呈黄色 | 溶液Y中含Na+ |
| C | 将Na2SO3固体样品溶液溶解,加入硝酸钡溶液,再加入稀硝酸 | 沉淀不溶解 | Na2SO3样品已变质 |
| D | 向FeSO4溶液中加入硫酸酸化的H2O2溶液 | 溶液变黄 | 氧化性:H2O2>Fe3+ |
| A. | A | B. | B | C. | C | D. | D |
1.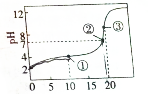 25℃时,向20mL0.2mo•lL-1HR溶液中逐渐滴入0.2mol•L-1NaOH溶液,得到如图的滴定曲线.下列粒子浓度的关系式错误的是( )
25℃时,向20mL0.2mo•lL-1HR溶液中逐渐滴入0.2mol•L-1NaOH溶液,得到如图的滴定曲线.下列粒子浓度的关系式错误的是( )
 25℃时,向20mL0.2mo•lL-1HR溶液中逐渐滴入0.2mol•L-1NaOH溶液,得到如图的滴定曲线.下列粒子浓度的关系式错误的是( )
25℃时,向20mL0.2mo•lL-1HR溶液中逐渐滴入0.2mol•L-1NaOH溶液,得到如图的滴定曲线.下列粒子浓度的关系式错误的是( )| A. | 点①溶液中,c(HR)+2c(H+)=c(R-)+2c(OH-) | |
| B. | 点②溶液中,c(Na+)=c(HR)+c(R-) | |
| C. | 点③溶液中,c(Na+)>c(R-)>(OH-)>c(H+) | |
| D. | 滴定过程中可能会出现,c(HR)>c(R-)>(H+)>c(Na+) |
19.实验室中需要配制2mol/L的NaOH溶液850mL,配制时应选用的容量瓶的规格和称取的NaOH的质量分别是( )
| A. | 950mL,76g | B. | 500mL,80g | C. | 1000mL,80g | D. | 1000mL,76g |