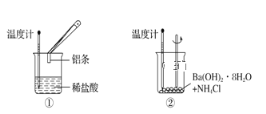
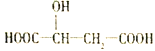题目内容
【题目】下列说法中正确的是
A. 6.8 g熔融KHSO4与3.9 g熔融Na2O2中阴离子数目相同
B. 某金属阳离子的结构示意图为![]() ,其与Cl-形成的强电解质都是离子化合物
,其与Cl-形成的强电解质都是离子化合物
C. 二硫化碳的电子式为![]()
D. 中子数为18的氯原子可表示为18Cl
【答案】A
【解析】
试题A、6.8g硫酸氢钾的物质的量是6.8g÷136g/mol=0.05mol,3.9g过氧化钠的物质的量是3.9g÷78g/mol=0.05mol,因此在熔融状态下硫酸氢钾与过氧化钠中阴阳离子的物质的量都是0.05mol,A正确;B、该金属阳离子也可能是铝离子,与氯离子形成的化合物氯化铝是共价化合物,B错误;C、二硫化碳是直线形非极性分子,其电子式为![]() ,C错误;D、中子数为18的氯原子可表示为35Cl,D错误,答案选A。
,C错误;D、中子数为18的氯原子可表示为35Cl,D错误,答案选A。

【题目】I.现有常温下pH=2的HCl溶液甲和pH=2的CH3COOH溶液乙,请根据下列操作回答问题:
(1)常温下0.1mol·L-1的CH3COOH溶液加水稀释过程中,下列表达式的数据一定变小的是_____。
A.c(H+) B.![]() C.c(H+)·c(OH-)
C.c(H+)·c(OH-)
(2)取10mL的乙溶液,加入等体积的水,CH3COOH的电离平衡________(填“向左”“向右”或“不”)移动;另取10mL的乙溶液,加入少量无水醋酸钠固体(假设加入固体前后溶液体积保持不变),待固体溶解后,溶液中![]() 的比值将________(填“增大”“减小”或“无法确定”)。
的比值将________(填“增大”“减小”或“无法确定”)。
(3)取等体积的甲、乙两溶液,分别用等浓度的NaOH稀溶液中和,则消耗NaOH溶液体积的大小关系为V(甲)________(填“>”“<”或“=”)V(乙)。
(4)已知25℃时,下列酸的电离平衡常数如下:
化学式 | CH3COOH | H2CO3 | HClO |
电离平衡常数 | 1.8×10-5 | K1=4.3×10-7 K2=4.7×10-11 | 3.0×10-8 |
下列四种离子结合H+能力最强的是________。
A.HCO B.CO![]() C.ClO- D.CH3COO-
C.ClO- D.CH3COO-
写出下列反应的离子方程式:HClO+Na2CO3(少量):______________________
II.室温下,0.1 mol·L-l的KOH溶液滴10.00mL 0.10 mol·L-l H2C2O4 (二元弱酸)溶液,所得滴定曲线如图(混合溶液的体积可看成混合前溶液的体积之和)。请回答下列问题:
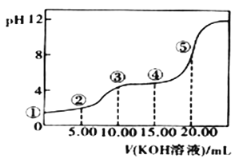
(5)点③所示溶液中所有离子的浓度由大到小的顺序为:________________________。点④所示溶液中:c(K+)+c(H2C2O4)+c(HC2O4)+c(C2O42)=________mol/L。