题目内容
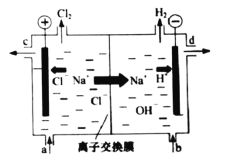
【题目】由于Fe(OH)2极易被氧化,所以实验室很难用亚铁盐溶液与烧碱反应制得白色纯净的Fe(OH)2沉淀。若用如图所示实验装置则可制得纯净的Fe(OH)2沉淀, 两极材料分别为石墨和铁。

①a电极材料为_______,该电极的电极反应式为________.
②若白色沉淀在电极周围生成,则电解液d是____(填序号,下同);若白色沉淀在两极之间的溶液中生成,则电解液d是____。
A.纯水 B.NaCl溶液 C.NaOH溶液D.CuCl2溶液
③液体c为苯,其作用是__________
④要想尽早在两极之间的溶液中看到白色沉淀, 可以采取的措施是(_______)
A.改用稀硫酸作电解 B.适当增大电源电压 C.适当降低电解液温度
【答案】Fe Fe-2e-=Fe2+ C B 隔绝空气,防止白色沉淀被氧化 B
【解析】
①该装置为制备纯净Fe(OH)2沉淀的装置,则Fe作阳极,即a电极为Fe,发生的电极反应为:Fe-2e-=Fe2+,故答案为:Fe;Fe-2e-=Fe2+;
②A.纯水几乎不导电,不可作电解液,A不满足题意;
B.电解质液为NaCl溶液时,阳极反应为水电离的H+得电子产生OH-,OH-和Fe2+迁移后在两极之间的溶液产生白色Fe(OH)2沉淀,B满足白色沉淀在两极之间的溶液中生成;
C.电解质液为NaOH溶液,Fe电极附近有高浓度的OH-,白色沉淀在Fe电极负极产生,C满足色沉淀在电极周围生成;
D.电解质液为CuCl2溶液,阴极为Cu2+得电子得到Cu,不产生白色Fe(OH)2沉淀,D不满足题意;
故答案为:C;B;
③苯不溶于水,密度比水小,浮在电解液表面,可隔绝空气,防止白色沉淀被氧化,故答案为:隔绝空气,防止白色沉淀被氧化;
④A.改用稀硫酸作电解,稀硫酸为强酸,不会产生白色Fe(OH)2沉淀,A不满足题意;
B.适当增大电源电压,反应速率加快,可尽早在两极之间的溶液中看到白色沉淀,B满足题意;
C.降低电解液温度,反应速率减小,看到白色沉淀的时间变长,C不满足题意;
故答案为:B。

【题目】已知海水提取镁的主要步骤如下:
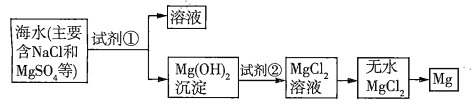
(1)关于加入试剂①作沉淀剂,有以下方法,请完成下列问题。
方法 | 是否合理 | 简述理由 |
方法:高温加热蒸发海水后,再加入沉淀剂 | a | b |
你认为合理的其他方法是c |
a. _____________;
b.____________;
c.____________。
(2)框图中加入的试剂①应该是_______(填物质名称),加入试剂②的溶质是_______(填化学式)。工业上由无水![]() 制取镁的化学方程式为___________。
制取镁的化学方程式为___________。