题目内容
【题目】在3个容积均为10L的密闭容器中分别放入0.2mol PCl3和0.2 molCl2,在不同条件下发生反应PCl3(g)+Cl2(g)![]() PCl5(g)。各容器内气体总压强随时间的变化如图所示。
PCl5(g)。各容器内气体总压强随时间的变化如图所示。
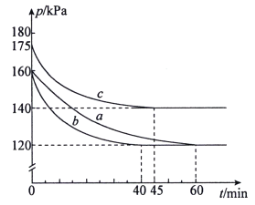
下列说法错误的是
A.实验a从反应开始至达到平衡时的平均速率v(Cl2)=![]() mol·L-1·min-1
mol·L-1·min-1
B.与实验a相比,实验b使用了催化剂,实验c是在较高温度下进行的
C.实验c中反应的平衡常数为![]() L·mol-1
L·mol-1
D.三组实验中反应的平衡转化率:a=b>c
【答案】C
【解析】
恒温恒容条件下,气体压强之比等于气体物质的量之比,设到平衡状态时消耗PCl3物质的量为x,则三段式:
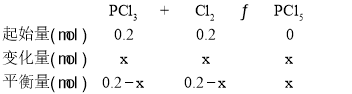
A. 实验a气体压强160变化为120,60min达到平衡状态,气体压强之比等于气体物质的量之比,0.4:(0.4-x)=160:120,解得:x=0.1,则实验a从反应开始至达到平衡时的反应速率为: ,A正确;
,A正确;
B. 分析图象可知,达到平衡状态的时间不同,时间越短反应速率越快,从反应开始至达到平衡时的反应速率v(PCl3)由大到小的次序b>c>a,实验b与实验a相比,达到相同平衡状态,但时间不同,实验b改变的实验条件是加入了催化剂改变了反应速率,实验c是在较高温度下进行的,B正确;
C. 实验c气体压强175变化为140,45 min达到平衡状态,气体压强之比等于气体物质的量之比,0.4:(0.4-x)=175:140,解得:x=0.08,平衡常数![]() ,C错误;
,C错误;
D. 实验b与实验a相比,实验b用了催化剂加快反应速率,实验a与实验b的转化率相同,根据A的计算,实验a的转化率![]() ,根据C的计算,实验c的转化率
,根据C的计算,实验c的转化率![]() ,所以三组实验中反应的平衡转化率:a=b>c,D正确;故答案为:C。
,所以三组实验中反应的平衡转化率:a=b>c,D正确;故答案为:C。

练习册系列答案
 优加精卷系列答案
优加精卷系列答案
相关题目