题目内容
【题目】化学实验在学科中有着非常重要的作用,结合图示实验装置,下列相关分析的描述不正确的是( )
A.图1:盐桥中使用KCl溶液,电子的流向是Zn→G→Cu→CuSO4溶液→盐桥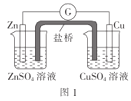
B.图2:可根据该实验验证铁的吸氧腐蚀
C.图3:在强酸和强碱的中和热实验中,强碱的浓度比强酸的略大
D.图4:根据两烧瓶中气体颜色的变化(热水中变深、冰水中变浅)可以判断反应2NO2(g)![]() N2O4(g)是一个放热反应
N2O4(g)是一个放热反应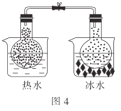
【答案】A
【解析】
A.图1表示的Zn-Cu原电池,Zn失去电子,作负极,电子经过外电,达到正极,电子流向为Zn→G→Cu,但是电子不能经过电解质溶液,也不能经过盐桥,错误,A符合题意;
B.若发生吸氧腐蚀,O2+4e-+2H2O=4OH-,装置中氧气的量减少,右侧导管中的液面会上升,可以证明发生了吸氧腐蚀,正确,B不符合题意;
C.在进行中和热的测定实验时,为了保证强酸完全反应掉,强碱的浓度会比强酸的略大,正确,C不符合题意;
D.根据图示,热水中的烧瓶的颜色更深,NO2的含量很多,可知,升高温度,平衡向着生成NO2的方向移动,则生成NO2的方向为吸热反应方向,可知2NO2(g)![]() N2O4(g)是一个放热反应,正确,D不符合题意。
N2O4(g)是一个放热反应,正确,D不符合题意。
答案选A。

 名校通行证有效作业系列答案
名校通行证有效作业系列答案【题目】室温下,1 L含0.1 mol HA和0.1 mol NaA的溶液a及加入一定量强酸或强碱后溶液的pH如下表(加入前后溶液体积不变):
溶液a | 通入0.01 mol HCl | 加入0.01 mol NaOH | |
pH | 4.76 | 4.67 | 4.85 |
像溶液a这样,加入少量强酸或强碱后pH变化不大的溶液称为缓冲溶液。
下列说法正确的是
A.溶液a和 0.1 mol·L1 HA溶液中H2O的电离程度前者小于后者
B.向溶液a中通入0.1 mol HCl时,A结合H+生成 HA,pH变化不大
C.该温度下HA的Ka=10-4.76
D.含0.1 mol·L1 Na2HPO4 与0.1 mol·L1 NaH2PO4的混合溶液也可做缓冲溶液


