题目内容
【题目】环境监察局常用“定电位NOx传感器来监测化工厂的氮氧化物气体是否达到排放标准,其工作原理如图所示。下列说法不正确的是( )

A.“对电极”是负极
B.“工作电极”上发生的电极反应为NO2+2e-+2H+=NO+H2O
C.传感器工作时H+移向“对电极”
D.“对电极”的材料可能为活泼金属锌
【答案】C
【解析】
A.“工作电极”通入NO2生成NO,说明NO2被还原,为原电池正极,则“对电极”是负极,故A正确;
B.“工作电极”通入NO2生成NO,为原电池正极,电极反应式为NO2+2e-+2H+=NO+H2O,故B正确;
C.阳离子向正极移动,所以传感器工作时H+移向“工作电极”,故C错误;
D.根据以上分析可知,“对电极”是负极,则“对电极”的材料可能为活泼金属锌,故D正确;
故答案为C。

练习册系列答案
相关题目
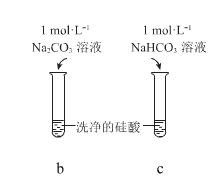
【题目】硅酸(H2SiO3)是一种难溶于水的弱酸,从溶液中析出时常形成凝胶状沉淀。实验室常用 Na2SiO3 溶液制备硅酸。某小组同学进行了如下实验:
编号 | Ⅰ | Ⅱ |
实验 |
|
|
现象 | a 中产生凝胶状沉淀 | b 中凝胶状沉淀溶解,c 中无明显变化 |
下列结论不正确的是
A.Na2SiO3 溶液一定显碱性
B.由 Ⅰ 不 能 说 明 酸 性 H2CO3>H2SiO3
C.由Ⅱ可知,同浓度时 Na2CO3 溶液的碱性强于 NaHCO3 溶液
D.向 Na2SiO3 溶液中通入过量 CO2,发生反应:SiO32-+CO2+H2O=CO32-+H2SiO3↓