题目内容
【题目】利用![]() 溶液、尿素
溶液、尿素![]() 为原料制取水合肼
为原料制取水合肼![]() 的流程如下:
的流程如下:
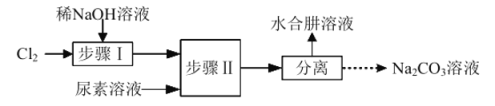
已知:①![]()
②![]() 沸点约
沸点约![]() ,具有强还原性,能与
,具有强还原性,能与![]() 剧烈反应生成
剧烈反应生成![]() 。
。
下列说法错误的是( )
A.步骤Ⅰ、Ⅱ反应过程中需控制好温度
B.所得副产物![]() 可用于工业上吸收
可用于工业上吸收![]() 尾气
尾气
C.步骤Ⅱ具体操作为将尿素溶液逐滴加入![]() 溶液中
溶液中
D.水合肼与![]() 反应的离子方程式为:
反应的离子方程式为:![]() ↑
↑
【答案】C
【解析】
实验流程可知步骤I为氯气和氢氧化钠溶液的反应,生成NaClO,为避免生成NaClO3,应控制温度在40![]() 以下,生成的NaClO与尿素反应生成N2H4H2O和Na2CO3,可用蒸馏的方法分离出N2H4H2O,副产品Na2CO3溶液中通入二氧化硫,可制得Na2SO3。
以下,生成的NaClO与尿素反应生成N2H4H2O和Na2CO3,可用蒸馏的方法分离出N2H4H2O,副产品Na2CO3溶液中通入二氧化硫,可制得Na2SO3。
A. 步骤I制备NaClO溶液时,若温度超过40![]() ,Cl2与NaOH溶液反应生成NaClO3和NaC1,步骤Ⅱ中NaClO碱性溶液与尿素水溶液在40
,Cl2与NaOH溶液反应生成NaClO3和NaC1,步骤Ⅱ中NaClO碱性溶液与尿素水溶液在40![]() 以下反应,所以步骤Ⅰ、Ⅱ反应过程中需控制好温度,A正确;
以下反应,所以步骤Ⅰ、Ⅱ反应过程中需控制好温度,A正确;
B. 副产品Na2CO3溶液中通入二氧化硫,可制得Na2SO3,可以用于吸收![]() 尾气,B正确;
尾气,B正确;
C. 步骤Ⅱ的反应为NaClO碱性溶液与尿素反应制备水合肼,由于水合肼具有强还原性,能与NaClO剧烈反应生成氮气,为了防止水合肼被氧化,应逐滴滴加NaClO碱性溶液,C错误;
D. 水合肼被![]() 氧化生成氮气,其反应的离子方程式为:
氧化生成氮气,其反应的离子方程式为:![]() ↑,D正确;故答案为:C。
↑,D正确;故答案为:C。

 100分闯关期末冲刺系列答案
100分闯关期末冲刺系列答案 名校联盟快乐课堂系列答案
名校联盟快乐课堂系列答案【题目】下列有关水溶液中的平衡相关的问题,请填空
(1)已知常温下,将氯化铝溶液和碳酸钠溶液混合,有白色沉淀产生,写出反应离子方程式______________
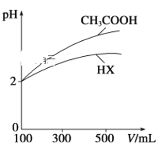
(2)体积均为100 mL、pH均为2的CH3COOH与一元酸HX,加水稀释过程中pH与溶液体积的关系如图所示。同浓度,同体积的CH3COONa与NaX溶液,离子总数目: CH3COONa溶液_______NaX溶液(填>,<,=)
(3)电离平衡常数是衡量弱电解质电离程度强弱的物理量。已知:
化学式 | 电离常数(25 ℃) |
HCN | K=4.9×10-10 |
CH3COOH | K=1.8×10-5 |
①25℃时,浓度均为0.01 mol·L-1 HCN和NaCN混合溶液显_____性(填酸,碱,中)。溶液中HCN浓度_________CN-浓度(填>,<,=)
②25 ℃时,在CH3COOH与CH3COONa的混合溶液中,若测得pH=6,则溶液中![]() =____。
=____。
(4)在25°C下,将x mol·L-1的氨水与y mol·L-1的盐酸等体积混合,反应后溶液中显中性,则c(NH4+)____c(Cl-)(填“>” 、“<” 或“=” );用含x和y的代数式表示出氨水的电离平衡常数______。