题目内容
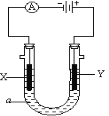
【题目】关于如图所示转化关系(X代表卤素),下列说法正确的是( )

A.![]()
B.![]()
C.![]() 的非金属性依次减弱,所以途径II吸收的热量依次增多
的非金属性依次减弱,所以途径II吸收的热量依次增多
D.生成相同物质的量![]() 放出的热量比生成
放出的热量比生成![]() 的多,说明
的多,说明![]() 比
比![]() 稳定
稳定
【答案】D
【解析】
A. 原子形成化学键放热,焓变小于0,则2H(g)+2X(g)═2HX(g) △H3<0,故A错误;
B. 反应焓变与起始物质和终了物质有关,与变化途径无关,途径Ⅰ生成HX的反应热与途径无关,所以△H1=△H2+△H3,故B错误;
C. Cl、Br、I的原子半径依次增大,非金属性逐渐减小,则Cl2、Br2、I2断裂化学键需要能量减小,所以途径Ⅱ吸收的热量依次减小,故C错误;
D. 因化学反应所吸收或放出的能量即为反应热,反应热等于反应中断裂旧化学键消耗的能量之和与形成新化学键放出的能量之和的差,氯原子半径小于溴原子,途径Ⅰ生成![]() 放出的热量比生成
放出的热量比生成![]() 的多,说明
的多,说明![]() 比
比![]() 稳定,故D正确;
稳定,故D正确;
故选D。

【题目】某工厂废液经测定得知主要含有乙醇,其中还含有丙酮、乙酸和乙酯乙酯。根据下表中各物质的性质,按下列步骤回收乙醇和乙酸。
已知:乙酸乙酯在碱性条件下水解生成乙酸钠和乙醇。
物质 | 丙酮 | 乙酸乙酯 | 乙醇 | 乙酸 |
沸点/℃ | 56.2 | 77.06 | 78.5 | 117.9 |
①向废液中加入烧碱溶液,调整溶液的pH=10;②将混合液放入蒸馏器中缓缓加热;③收集温度在70~85℃时的馏出物;④排出蒸馏器中的残液,冷却后向其中加浓硫酸(过量),然后再放入耐蒸馏器中进行蒸馏,回收馏出物。请回答下列问题:
(1)加入烧碱使溶液的pH=10的目的是_______________________。
(2)在70~85℃时馏出物的主要成分是________。
(3)在步骤④中加入过量浓硫酸的目的是(用化学方程式表示)_____________________。