题目内容
【题目】已知标准状况下CH4的体积为4.48L,该气体的物质的量为___________,分子数为___________, 原子数约为___________,质子数为___________,电子数为___________,摩尔质量为___________,质量为___________。
【答案】0.2mol 0.2NA 6.02×1023 2NA 2NA 16g/mol 3.2g
【解析】
根据公式![]() 进行计算。
进行计算。
标准状况下CH4的体积为4.48L,该气体的物质的量为![]() =0.2mol;0.2molCH4的分子数为
=0.2mol;0.2molCH4的分子数为![]() =0.2NA;1个CH4分子中,有5个原子,10个质子和10个电子,则0.2 NA 的CH4的原子数约为
=0.2NA;1个CH4分子中,有5个原子,10个质子和10个电子,则0.2 NA 的CH4的原子数约为![]() ,质子数等于电子数等于
,质子数等于电子数等于![]() ;CH4的相对分子质量为16,则摩尔质量为16g/mol,0.2molCH4的质量
;CH4的相对分子质量为16,则摩尔质量为16g/mol,0.2molCH4的质量![]() =3.2g,故答案为:0.2mol;0.2NA ;6.02×1023 ;2NA;2NA ; 16g/mol;3.2g。
=3.2g,故答案为:0.2mol;0.2NA ;6.02×1023 ;2NA;2NA ; 16g/mol;3.2g。

练习册系列答案
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案
相关题目
【题目】一定温度下,向1.0L的密闭容器中加入0.60molX(g),发生反应X(g)![]() Y(s)+2Z(g),测得反应物X的浓度与反应时间的关系如表所示:
Y(s)+2Z(g),测得反应物X的浓度与反应时间的关系如表所示:
反应时间t/min | 0 | 1 | 2 | 3 | 4 | 6 | 8 |
c(X)/(mol·L-1) | 0.60 | 0.42 | 0.30 | 0.21 | 0.15 | a | 0.0375 |
(1)0~3min内用Z表示的平均反应速度v(Z)=___。
(2)分析该反应中反应物的浓度与时间的关系,得出的结论是___。由此规律推出在6min时反应物X的浓度为___mol·L-1。
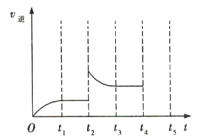
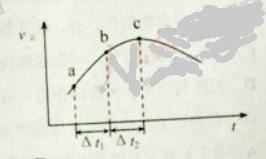
(3)该反应的逆反应速率随时间变化的曲线如图所示,t2时改变的条件可能是___、___。