题目内容
【题目】优化反应条件是研究化学反应的重要方向。
(1)以硫代硫酸钠与硫酸的反应Na2S2O3 + H2SO4= Na2SO4 + SO2+ S↓ + H2O为例,探究外界条件对化学反应速率的影响,实验方案如下表所示。
实验 序号 | Na2S2O3溶液 | H2SO4溶液 | 蒸馏水 | 温度/℃ | ||
浓度/(mol/L) | 体积/mL | 浓度/(mol/L) | 体积/mL | 体积/mL | ||
I | 0.1 | 1.5 | 0.1 | 1.5 | 10 | 20 |
II | 0.1 | 2.5 | 0.1 | 1.5 | 9 | a |
III | 0.1 | b | 0.1 | 1.5 | 9 | 30 |
①表中,a为________________________,b为________________。
②实验表明,实验III的反应速率最快,支持这一结论的实验现象为_________________________。
(2)硫代硫酸钠可用于从含氧化银的矿渣中浸出银,反应如下:Ag2O + 4S2O32- + H2O ![]() 2[Ag(S2O3)2]3- + 2OH-,实际生产中,为了提高银的浸出率需要调节pH的范围为8.5~9.5,解释其原因________
2[Ag(S2O3)2]3- + 2OH-,实际生产中,为了提高银的浸出率需要调节pH的范围为8.5~9.5,解释其原因________
(3)工业上常用空气催化氧化法除去电石渣浆(含CaO)上清液中的S2-,并制取石膏(CaSO4·2H2O),其中的物质转化过程如下图所示。
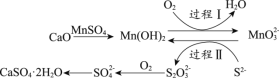
①过程I、II中,起催化剂作用的物质是_______________。
②过程II中,反应的离子方程式为_________。
③根据物质转化过程,若将10 L上清液中的S2-转化为SO42-(S2-浓度为320 mg/L),理论上共需要标准状况下的O2的体积为___________L。
【答案】20 2.5 实验III中出现浑浊所需时间最短 若pH小于8.5,c(H+)增大,H+与S2O32-反应使c(S2O32-)减小,不利于反应正向进行,浸出率下降;若pH大于9.5,c(OH-)增大,不利于反应正向进行,浸出率下降 Mn(OH)2 4MnO32- +2S2- + 9H2O = S2O32- + 4Mn(OH)2↓ + 10OH- 4.48
【解析】
(1)①探究反应速率的影响遵循控制变量的思想,实验I和实验II中溶液的体积不同,则温度应相同,则a为20,实验II和实验III,温度不同,则其他变量应相同,则b为2.5,
答案为:20;2.5;
②根据反应Na2S2O3 + H2SO4= Na2SO4 + SO2+ S↓ + H2O可知,通过实验现象能表现出反应快慢的现象是产生硫沉淀的速度,硫沉淀出现越快表明反应速率越快,能表明实验III的反应速率最快的实验现象为出现浑浊所需时间最短,
答案为:实验III中出现浑浊所需时间最短;
(2)根据Ag2O + 4S2O32- + H2O ![]() 2[Ag(S2O3)2]3- + 2OH-为可逆反应,若pH小于8.5,c(H+)增大,H+与S2O32-反应使c(S2O32-)减小,不利于反应正向进行,浸出率下降;若pH大于9.5,c(OH-)增大,不利于反应正向进行,浸出率下降,
2[Ag(S2O3)2]3- + 2OH-为可逆反应,若pH小于8.5,c(H+)增大,H+与S2O32-反应使c(S2O32-)减小,不利于反应正向进行,浸出率下降;若pH大于9.5,c(OH-)增大,不利于反应正向进行,浸出率下降,
答案为:若pH小于8.5,c(H+)增大,H+与S2O32-反应使c(S2O32-)减小,不利于反应正向进行,浸出率下降;若pH大于9.5,c(OH-)增大,不利于反应正向进行,浸出率下降;
(3)①根据过程I、II中的转化关系,起催化剂作用的物质是Mn(OH)2,
答案为:Mn(OH)2;
②根据转化关系图,过程II中S2-与MnO32-生成S2O32-和Mn(OH)2,根据氧化还原反应得失电子守恒和物料守恒,反应的离子方程式为4MnO32- +2S2- + 9H2O = S2O32- + 4Mn(OH)2↓ + 10OH-,
③10 L上清液中的S2-的物质的量=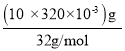 =0.1mol,根据物质转化过程,S2-转化为S2O32-过程中需要消耗氧气,S2O32-转化为SO42-也需要消耗氧气,0.1mol S2-转化为S2O32-时,硫元素的化合价由-2价变为+2,共失去0.1mol×4=0.4mol电子;氧气转变为水时氧元素由0价变为-2价,即1mol氧气转移4mol电子,根据电子得失守恒,得到0.4mol电子需要氧气的物质的量=
=0.1mol,根据物质转化过程,S2-转化为S2O32-过程中需要消耗氧气,S2O32-转化为SO42-也需要消耗氧气,0.1mol S2-转化为S2O32-时,硫元素的化合价由-2价变为+2,共失去0.1mol×4=0.4mol电子;氧气转变为水时氧元素由0价变为-2价,即1mol氧气转移4mol电子,根据电子得失守恒,得到0.4mol电子需要氧气的物质的量=![]() =0.1mol;根据反应4MnO32- +2S2- + 9H2O = S2O32- + 4Mn(OH)2↓ + 10OH-,0.1mol S2-参与反应生成S2O32-的物质的量=
=0.1mol;根据反应4MnO32- +2S2- + 9H2O = S2O32- + 4Mn(OH)2↓ + 10OH-,0.1mol S2-参与反应生成S2O32-的物质的量=![]() ×0.1mol=0.05mol,0.05mol S2O32-转化为SO42-,硫元素的化合价由+2价变为+6价,共失去0.05mol×2×4=0.4mol电子,氧气由0价变为-2价,即1mol氧气转移4mol电子,根据电子得失守恒,得到0.4mol电子需要氧气的物质的量=
×0.1mol=0.05mol,0.05mol S2O32-转化为SO42-,硫元素的化合价由+2价变为+6价,共失去0.05mol×2×4=0.4mol电子,氧气由0价变为-2价,即1mol氧气转移4mol电子,根据电子得失守恒,得到0.4mol电子需要氧气的物质的量=![]() =0.1mol;则上清液中的S2-转化为SO42-过程中一共需要氧气的物质的量=0.1mol+0.1mol=0.2mol,标准状况下的O2的体积=0.2mol×22.4L/mol=4.48L,
=0.1mol;则上清液中的S2-转化为SO42-过程中一共需要氧气的物质的量=0.1mol+0.1mol=0.2mol,标准状况下的O2的体积=0.2mol×22.4L/mol=4.48L,
答案为:4.48。

 全能测控一本好卷系列答案
全能测控一本好卷系列答案