题目内容
8.浓硫酸在与含有水分的蔗糖作用过程中没有显示的性质是( )| A. | 强氧化性 | B. | 脱水性 | C. | 酸性 | D. | 吸水性 |
分析 浓硫酸属于酸,具有酸的性质,同时还具有吸水性、脱水性和强氧化性,能将有机物中H、O元素以2:1水的形式脱去而体现脱水性,据此分析解答.
解答 解:浓硫酸和含有水分的蔗糖作用,被脱水后生成了黑色的炭(碳化),并会产生二氧化硫. 反应过程分两步,浓硫酸吸收水,蔗糖(C12H22O11)在浓硫酸作用下脱水,生成碳和水(试验后蔗糖会变黑,黑的就是碳颗粒),这一过程表现了浓硫酸的吸水性和脱水性:第二步,脱水反应产生的大量热让浓硫酸和C发生反应生成二氧化碳和二氧化硫,这一过程表现了浓硫酸的强氧化性,
故选C.
点评 本题考查浓硫酸的性质,浓硫酸具有酸性、吸水性、脱水性和强氧化性,注意吸水性和脱水性区别,题目难度不大.

练习册系列答案
相关题目
18.一定条件下反应N2(g)+3H2(g)?2NH3(g)在10L的密闭容器中进行,测得2min内,N2的物质的量由20mol减小到8mol,则2min内NH3的反应速率为( )
| A. | 1mol•L-1•min-1 | B. | 1.2mol•L-1•min-1 | ||
| C. | 6mol•L-1•min-1 | D. | 0.41mol•L-1•min-1 |
19.Na、Fe、C、O、Si、Cl是中学化学中常见的六种元素.
(1)Si位于元素周期表第三周期第ⅣA族;Fe的基态原子外围电子层排布式为3d64s2.
(2)用“>”或“<”或元素符号填空:
(3)已知甲醇的燃烧热为726.5kJ/mol,写出甲醇燃烧的热化学方程式.CH3OH(l)+$\frac{3}{2}$O2(g)=CO2(g)+H2O(l)△H=-726.5kJ/mol.
(4)FeO42- 具有强氧化性,在其钠盐溶液中加入稀硫酸,溶液变为黄色,并有无色气体产生.该反应的离子方程式为4 FeO42-+20 H+=4Fe3++3O2↑+10H2O.
(1)Si位于元素周期表第三周期第ⅣA族;Fe的基态原子外围电子层排布式为3d64s2.
(2)用“>”或“<”或元素符号填空:
| C、O、Si第一电离能 | 离子半径Cl-、Na+、O2- | 熔点 | 电负性 |
| Si<C<O | Cl->O2->Na+ | CO2<SiO2 | Cl>Si |
(4)FeO42- 具有强氧化性,在其钠盐溶液中加入稀硫酸,溶液变为黄色,并有无色气体产生.该反应的离子方程式为4 FeO42-+20 H+=4Fe3++3O2↑+10H2O.
3.海水淡化是指除去海水中的盐分以获得淡水的工艺过程,其方法较多,如反渗透法、电渗析法、离子交换法等,下列方法中也是用来进行海水淡化的是( )
| A. | 过滤法 | B. | 萃取法 | C. | 分液法 | D. | 蒸馏法 |
13.X、Y、Z均为短周期元索,X、Y处于同一周期,X、Z的最低价离子分别为X2-和Z-,Y+和Z-具有相同的电子层结构.下列说法正确的是( )
| A. | 原子最外层电子数:X>Y>Z | B. | 单质活泼性:X>Y>Z | ||
| C. | 原子序数:X>Y>Z | D. | 离子半径:X2->Y+>Z- |
20.化学与生活密切相关,下列说法不正确的是( )
| A. | 用热的纯碱溶液可洗涤餐具上的油污 | |
| B. | 新制Cu(OH)2悬浊液在医院中常用于尿糖的检测 | |
| C. | 用灼烧并闻气味的方法可区别棉麻织物和纯羊毛织物 | |
| D. | 煤经过气化和液化等物理变化可以转化为清洁燃料 |
17.已知维生素A的结构简式如图,关于它的说法正确的是( )
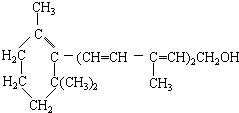
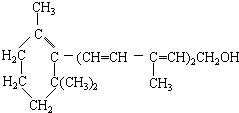
| A. | 维生素A分子含有氢原子数为奇数 | |
| B. | 维生素A的分子中含有苯环结构 | |
| C. | 1mol维生素A在催化剂作用下,可以和5molH2完全加成 | |
| D. | 维生素A属于醇,是一种水溶性维生素,可以发生消去反应 |
18.常温下的4种混合溶液,分别由等体积0.1mol/L的2种溶液混合而成
①NH4Cl与NaOH ②NH4Cl与HCl ③NH4Cl与NaCl ④NH4Cl与NaHCO3
下列各项正确的是( )
①NH4Cl与NaOH ②NH4Cl与HCl ③NH4Cl与NaCl ④NH4Cl与NaHCO3
下列各项正确的是( )
| A. | PH大小顺序①>④>③>② | |
| B. | C(NH3•H2O)大小顺序:②>④>③>① | |
| C. | 混合溶液④中存在C(NH3•H2O)+C(CO32-)+C(H+)=C(OH-)+C(H2CO3) | |
| D. | 混合溶液③中水的电离被促进,其中C(H+)和C(OH-)均大于1.0×10-7mol/L |
 .
.