题目内容
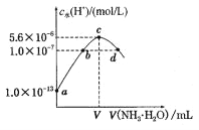
【题目】R、X、Y、Z是短周期元素,原子序数依次增大。R是自然界中组成物质种类最多的元素,R原子最外层电子数是X原子最外层电子数2倍。Z的最高价氧化物对应的水化物(M)是强电解质,向含Y元素的钠盐溶液中滴加M溶液,产生沉淀的物质的量与M的物质的量关系如图所示。下列推断正确的是
A. R的氢化物可能使溴水或酸性高锰酸钾溶液褪色
B. Y的气态氢化物热稳定性比R的强
C. 常温常压下,Z的单质一定呈黄绿色
D. X和Z组成的化合物属于共价化合物
【答案】A
【解析】
R是自然界组成物质最多的元素,所以R是碳,X的原子序数是R的2倍,X为镁,Z的最高价氧化物对应的水化物(M)是强电解质,向Y的钠盐溶液中滴加M溶液,产生沉淀为为Y的氧化物的水化物,最终沉淀不溶解,因此沉淀为硅酸,故Y是硅。硫酸和高氯酸都是强电解质,Z可能是硫、氯;故R是碳、X是镁、Y是硅、Z可能是馏或氯。
A.R 是碳,碳的氢化物属于烃类,烯烃、炔烃等能使溴水或酸性高锰酸钾溶液褪色,故A正确;
B.R是碳,Y是硅,碳的非金属性比硅强,甲烷比硅烷稳定,故B错误;
C.Z的单质可能是硫,也可能是氯气,只有氯气呈黄绿色,故C错误;
D.硫化镁、氯化镁都是离子化合物,故D错误;
本题答案为A。

 阅读快车系列答案
阅读快车系列答案【题目】工业合成氨的反应如下:3H2+N2![]() 2NH3。某温度下,在容积恒定为2.0 L的密闭容器中充入2.0 mol N2和2.0 mol H2,一段时间后反应达平衡状态,实验数据如下表所示:
2NH3。某温度下,在容积恒定为2.0 L的密闭容器中充入2.0 mol N2和2.0 mol H2,一段时间后反应达平衡状态,实验数据如下表所示:
t/s | 0 | 50 | 150 | 250 | 350 |
n(NH3)/mol | 0 | 0.24 | 0.36 | 0.40 | 0.40 |
(1)0~50 s内的平均反应速率 v(N2)=_______________。
(2)250 s时,H2的转化率为_______________。
(3)已知N≡N的键能为946 kJ·mol-1,H-H的键能为436 kJ·mol-1,N-H的键能为391 kJ·mol-1,则生成1 mol NH3过程中的热量变化为_______kJ。下图能正确表示该反应中能量变化的是_____(填字母)。
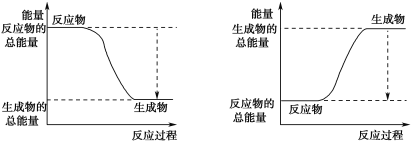
A B
(4)为加快反应速率,可以采取的措施______________。
a.降低温度 b.增大压强 c.恒容时充入He气
d.恒压时充入He气 e.及时分离出NH3
(5)下列说法错误的是____________。
a.使用催化剂是为了加快反应速率,提高生产效率
b.上述条件下,N2不可能100%转化为NH3
c.在一定条件下,合成氨反应有一定的限度
d.250~350 s时,生成物浓度保持不变,反应停止
【题目】根据下列实验操作和现象能推出相应结论的是
选项 | 实验操作和现象 | 结论 |
A | 向NaAlO2溶液中滴加NaHCO3 溶液,产生白色沉淀 | AlO2-与HCO3-发生了相互促进的水解反应 |
B | 向溶有SO2的BaCl2溶液中通入气体X,出现白色沉淀 | X不一定具有氧化性 |
C | 灼热的木炭加入浓硝酸中,放出红棕色气体 | 一定是木炭与浓硝酸反应生成了NO2 |
D | 将乙醇与浓硫酸共热,制得的气体直接通入酸性KMnO4溶液中,酸性KMnO4溶液褪色 | 说明制得的气体中含有乙烯 |
A. A B. B C. C D. D