题目内容
【题目】一定量的甲烷燃烧后得到的产物为CO、CO 2 和水蒸气,此混合气体质量为 49.6 g ,当其缓慢经过无水氯化钙(足量)时,氯化钙增重 25.2 g ,则原混合气体中CO 的质量为( )
A. 26.4 g B. 19.7 g C. 13.2 g D. 11.2 g
【答案】D
【解析】无水CaCl2增重25.2克,则水的质量为25.2g;
所以n(H2O)=![]() =1.4mol.
=1.4mol.
根据H原子守恒可计算CH4的物质的量为n(CH4)=![]() n(H2O)=
n(H2O)=![]() ×1.4mol=0.7mol.
×1.4mol=0.7mol.
根据C原子守恒可知CO和CO2的总的物质的量为0.7mol,
由于水的质量为25.2g,所以一氧化碳和二氧化碳的质量为:49.6g-25.2g=24.4g;
令CO、CO2的物质的量分别为xmol、ymol,则:
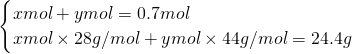
解得x=0.4,y=0.3.
所以原混合气中CO的质量为0.4mol×28g/mol=11.2g,故D正确。

【题目】实验室模拟合成硫酸的流程如下:

从下图中选择制取气体的合适装置:

(1)装置C的名称为_________________,实验室通常能用装置C制备_________。
A.H2 B.H2S C.CO2 D.O2
(2)实验室用装置D制备NH3的化学方程式为_______________________________。
(3)若用装置B制备SO2,可以选用试剂为___________。
A、浓硫酸、亚硫酸钠固体 B.浓硫酸、铜片
C.稀硫酸、亚硫酸溶液 D.浓硫酸、铁屑
(4)SO2和O2通过甲装置,甲装置的作用除了可以控制SO2、O2的流速外,还可以__________。

(5)若将一定量的SO2(g)和O2(g)分别通入到体积为2L的恒容密闭容器中,在不同温度下进行反应得到如下表中的两组数据:
实验编号 | 温度/℃ | 起始量/mol | 平衡量/mol | ||
SO2 | O2 | SO2 | O2 | ||
1 | T1 | 4 | 2 | x | 0.8 |
2 | T2 | 4 | 2 | 0.4 | y |
表中x=_______mol,y=_______mol,T1______T2(填“>”、“=”或“<”)
(6)SO2尾气可用NaOH溶液吸收,得到Na2SO3和NaHSO3两种盐。若一定物质的量的SO2与氢氧化钠溶液反应,所得溶液中Na2SO3和NaHSO3的物质的量之比为2:3,则参加反应的SO2和NaOH的物质的量之比为________。
A. 5:7 B.1:2 C.9:4 D.9:13
(7)硫酸与氨水反应生成硫酸铵或硫酸氢铵,现称取(NH4)2SO4和NH4HSO4混合物样品7.58 g,加入含0.1 molNaOH的溶液,发生反应:①OH-+H+→H2O, ②OH-+NH4+→NH3↑+H2O。充分反应,生成1792 mL(标准状况)。已知①优先反应,则样品中(NH4)2SO4的物质的量为_______mol,NH4HSO4的物质的量为_______mol。
