题目内容
【题目】如图为制取纯净干燥的Cl2并让其与铁发生反应的装置,A是Cl2发生装置,C、D为气体净化装置,E硬质玻璃管中装有细铁丝网;F为干燥的空广口瓶;烧杯G为尾气吸收装置.试回答: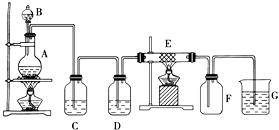
(1)C、G两个装置所盛放的试剂分别是:
CG .
(2)①装置搭好须进行气密性检查,写出操作方法: .
②两处酒精灯应先点燃处(填写A或B),目的是 .
③F中的现象为 , G中出现了一种沉淀,该沉淀的化学式 .
(3)写出在A、E中发生反应的化学方程式为:
A: .
E: .
【答案】
(1)饱和食盐水,氢氧化钠溶液
(2)关闭分液漏斗活塞,往烧杯G中加水,微热A处酒精灯,烧杯中有气泡产生,停止加热冷却后,导管中形成一段水柱,A,赶走空气,防止铁被空气氧化,产生棕黄或棕红或棕褐色的烟,Fe(OH)3
(3)MnO2+4HCl(浓) ![]() MnCl2+Cl2↑+2H2O,2Fe+3Cl2
MnCl2+Cl2↑+2H2O,2Fe+3Cl2 ![]() 2FeCl3
2FeCl3
【解析】解:(1)浓盐酸易挥发,制备的氯气中含有氯化氢,氯气在饱和氯化钠溶液中溶解度小,氯化氢易溶于水,可用饱和氯化钠溶液除去氯气中的氯化氢;氯气有毒,应进行尾气处理,氯气能够与氢氧化钠,被氢氧化钠溶液液吸收;
(2)①装置气密性检查方法:关闭分液漏斗活塞,往烧杯G中加水,微热A处酒精灯,烧杯中有气泡产生,停止加热冷却后,导管中形成一段水柱;
②装置中有空气,为防止空气中的氧气氧化铁,应先制备氯气,用氯气排尽装置中的空气,所以应先点燃A处酒精灯;
③铁与氯气反应生成氯化铁,F收集氯化铁,现象为:产生产生棕黄或棕红或棕褐色的烟;氯化铁与G中的氢氧化钠反应生成氢氧化铁沉淀;
(3)浓盐酸与二氧化锰在加热条件下反应生成氯化锰、氯气和水,化学方程式:MnO2+4HCl( 浓) ![]() MnCl2+Cl2↑+2H2O;
MnCl2+Cl2↑+2H2O;
铁在氯气中燃烧生成氯化铁,化学方程式:2Fe+3Cl2 ![]() 2FeCl3;
2FeCl3;
故答案为:(1)饱和食盐水;氢氧化钠溶液;(2)①关闭分液漏斗活塞,往烧杯G中加水,微热A处酒精灯,烧杯中有气泡产生,停止加热冷却后,导管中形成一段水柱;②A;赶走空气,防止铁被空气氧化;③产生棕黄或棕红或棕褐色的烟; Fe(OH)3;(3)MnO2+4HCl( 浓) ![]() MnCl2+Cl2↑+2H2O;2Fe+3Cl2
MnCl2+Cl2↑+2H2O;2Fe+3Cl2 ![]() 2FeCl3
2FeCl3
(1)C装置的作用主要用于除去氯气中混有的HCl;G装置主要用于尾气吸收,用NaOH溶液吸收多余的氯气。
(2)①检查装置气密性时,应先关闭分液漏斗活塞,通过装置AG的现象确定装置的气密性。
②铁的活动性较强,加热前应先排除装置内的空气。
③装置F中会有氯化铁生成;装置G的试剂为NaOH,易与FeCl3反应生成红褐色沉淀。
(3)装置A为实验室制取氯气的反应;装置E为铁与氯气的反应。