题目内容
1.液化石油气是石油化工生产过程中的一种副产品,也是常用的家用燃料,它的主要成分是丙烷、丁烷、丙烯、丁烯.下列说法中不正确的是( )| A. | 丙烷和丁烷互为同系物 | |
| B. | 丙烯和丁烯互为同系物 | |
| C. | 丙烷和丁烷中碳元素的质量分数相同 | |
| D. | 丙烯和丁烯中碳元素的质量分数相同 |
分析 同系物:结构相似,在分子组成上相差一个或若干个CH2原子团的物质互称为同系物,据此概念判断AB选项;
依据实验式相等,则不同烃中碳的质量分数相等解决CD即可.
解答 解:A、丙烷和丁烷均为饱和烷烃,符合通式CnH2n+2,属于同系物,故A正确;
B、丙烯和丁烯均为单烯烃,符合通式CnH2n,属于同系物,故B正确;
C、丙烷中碳元素质量分数为:$\frac{12×3}{12×3+8}$×100%=81.8%,丁烷中碳元素质量分数为:$\frac{12×4}{12×4+10}$×100%=82.7%,故两者不同,故C错误;
D、丙烯与丁烯的最简式均为CH2,故碳元素的质量分数相同,均为:$\frac{12}{12+2}$×100%=85.7%,故D正确,
故选C.
点评 本题主要考查的是同系物的概念、碳元素质量分数计算等,难度不大.

练习册系列答案
相关题目
11.下列关于乙炔制取的说法不正确的是( )
| A. | 为了加快反应速率可用饱和食盐水代替水反应 | |
| B. | 此反应是放热反应 | |
| C. | 反应中不需加碎瓷片作沸石 | |
| D. | 为了除去杂质气体,除了用硫酸铜外还可用氢氧化钠溶液 |
9.下列不属于影响离子晶体结构的因素是 ( )
| A. | 晶体中阴、阳离子的半径比 | B. | 离子晶体的晶格能 | ||
| C. | 晶体中阴、阳离子的电荷比 | D. | 离子键的纯粹程度 |
16.下列溶液中的离子反应表达正确的是( )
| A. | 将金属钠投入水中:Na+2H2O═Na++2OH-+H2↑ | |
| B. | 大理石与醋酸的反应:CaCO3+2H+═Ca2++CO2↑+H2O | |
| C. | 三氯化铁溶液中加入铜粉:Cu+Fe3+═Cu2++Fe2+ | |
| D. | 氯化铝溶液中加入过量的氨水:Al3++3NH3•H2O═Al(OH)3↓+3NH${\;}_{4}^{+}$ |
6.下列各对物质中,互为同系物的是( )
| A. | CH3-CH3和CH3-CH=CH2 | B. | CH3-CH=CH2和CH3-CH2-CH=CH2 | ||
| C. | 乙醇和丙三醇 | D. | 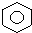 和 和 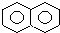 |
13.最近,科学家研制出一种纸质电池,这种“软电池”采用薄层纸片作为载体和传导体,在一边附着锌,在另一边附着二氧化锰.电池总反应为:Zn+2MnO2+H2O=ZnO+2MnO(OH).下列说法正确的是( )
| A. | 该电池Zn为负极,ZnO为正极,MnO2为催化剂 | |
| B. | 导电时外电路电子由Zn流向MnO2,内电路电子由MnO2流向Zn | |
| C. | 该电池的正极反应为:MnO2+e-+H2O=MnO(OH)+OH- | |
| D. | 电池工作时正极发生氧化反应 |
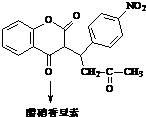
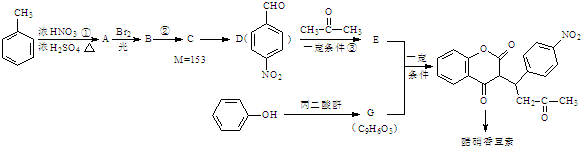
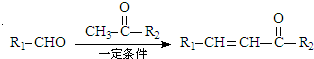 +H2O
+H2O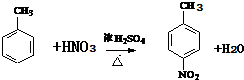 .
.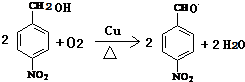 .
.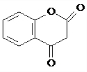 .
.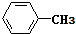 互为同系物;
互为同系物;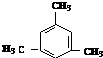 .
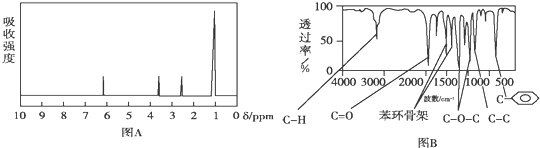
.
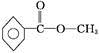 .
. ;该物质遇水剧烈反应,产生有刺激性气味的混合气体X和Y,同时还有固体单质产生,是已知X能使品红溶液褪色的气体,Y在标准状态下的密度为1.63g/L,该混合气体相对于H2的密度为21,上述过程对应的化学方程式为2S2Cl2+2H2O=SO2↑+4HCl+3S↓;某研究小组同学为确定干燥的X和Y混合气体中Y的存在,设计方案如下:把干燥的X和Y与干燥的NH3混合,出现白烟,则证明有Y气体,你认为此方案正确(填“正确”或“不正确”),理由是干燥的二氧化硫不与氨气反应,但干燥的氯化氢与氨气反应生成白烟.
;该物质遇水剧烈反应,产生有刺激性气味的混合气体X和Y,同时还有固体单质产生,是已知X能使品红溶液褪色的气体,Y在标准状态下的密度为1.63g/L,该混合气体相对于H2的密度为21,上述过程对应的化学方程式为2S2Cl2+2H2O=SO2↑+4HCl+3S↓;某研究小组同学为确定干燥的X和Y混合气体中Y的存在,设计方案如下:把干燥的X和Y与干燥的NH3混合,出现白烟,则证明有Y气体,你认为此方案正确(填“正确”或“不正确”),理由是干燥的二氧化硫不与氨气反应,但干燥的氯化氢与氨气反应生成白烟.