题目内容
11.有A、B、C、D四种有机物,A、B、C都属于烃类物质,D是烃的衍生物.A的球棍模型为 ;B的比例模型为
;B的比例模型为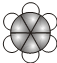 ;C是含氢量最大的有机物,分子结构为正四面体;D的相对分子质量为46,能与Na反应,但不能与NaOH溶液反应.
;C是含氢量最大的有机物,分子结构为正四面体;D的相对分子质量为46,能与Na反应,但不能与NaOH溶液反应.请回答下列问题:
(1)A、B、C、D的结构简式依次是:ACH3CH3,B
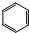 ,CCH4,DCH3CH2OH.
,CCH4,DCH3CH2OH.(2)上述物质中,苯(填名称)是无色带有特殊气味的液体,且有毒、不溶于水、密度比水小.向其中加入溴水,振荡静置后,观察到的现象是溶液分层,上层为橙色,下层无色.
(3)A与C互称为同系物,与它们分子组成和结构相似的有机物有一大类,均符合通式CnH2n+2,当n=5时,该有机物有3种同分异构体,写出其中碳链最短的同分异构体的结构简式C(CH3)4.
分析 A的球棍模型为 ,应为CH3CH3;B的比例模型为
,应为CH3CH3;B的比例模型为 ,为
,为 ;C是含氢量最大的有机物,分子结构为正四面体,应为CH4;D的相对分子质量为46,能与Na反应,但不能与NaOH溶液反应,说明含有羟基,应为CH3CH2OH,以此解答该题.
;C是含氢量最大的有机物,分子结构为正四面体,应为CH4;D的相对分子质量为46,能与Na反应,但不能与NaOH溶液反应,说明含有羟基,应为CH3CH2OH,以此解答该题.
解答 解:A的球棍模型为 ,应为CH3CH3;B的比例模型为
,应为CH3CH3;B的比例模型为 ,为
,为 ;C是含氢量最大的有机物,分子结构为正四面体,应为CH4;D的相对分子质量为46,能与Na反应,但不能与NaOH溶液反应,说明含有羟基,应为CH3CH2OH,
;C是含氢量最大的有机物,分子结构为正四面体,应为CH4;D的相对分子质量为46,能与Na反应,但不能与NaOH溶液反应,说明含有羟基,应为CH3CH2OH,
(1)由以上分析可知A、B、C、D的结构简式依次是CH3CH3、 、CH4、CH3CH2OH,故答案为:CH3CH3;
、CH4、CH3CH2OH,故答案为:CH3CH3; ;CH4;CH3CH2OH;
;CH4;CH3CH2OH;
(2)以上四种物质中,苯是无色带有特殊气味的液体,且有毒、不溶于水、密度比水小.向其中加入溴水,振荡静置后,溶液分层,上层为橙色,下层无色,
故答案为:苯;溶液分层,上层为橙色,下层无色;
(3)A与C互称为同系物,含5个碳原子的所有同分异构体的结构简式有:CH3CH2CH2CH2CH3、CH3CH(CH3)CH2CH3、C(CH3)4,共3种,其中C(CH3)4碳链最短,
故答案为:同系物;3;C(CH3)4.
点评 本题考查有机物推断,熟悉有机物结构、性质是解本题关键,为高频考点,侧重于学生的分析能力的考查,难点是同分异构体种类的判断,有碳链异构、官能团有关等,题目难度不大.

练习册系列答案
相关题目
1.下列实验操作能达到实验目的是( )
| 选项 | 实验操作 | 实验目的 |
| A | 向水解后的蔗糖溶液中直接加入新制的Cu(OH)2并加热 | 确定蔗糖是否发生水解 |
| B | 滴加KMnO4(H+)溶液,充分振荡 | 确定苯中混有己烯 |
| C | 加入金属钠 | 确定酒精中混有醋酸 |
| D | 加淀粉 | 确定KCl中含有KI |
| A. | A | B. | B | C. | C | D. | D |
2.生活中有不同纯度的水,其中纯度最高的是( )
| A. | 海水 | B. | 雨水 | C. | 蒸馏水 | D. | 自来水 |
19.下表列出了①~⑩十种元素在周期表中的位置:
(1)上述①~⑩十种元素中(用元素符号填空):构成有机物的主要元素是C,构成岩石与许多矿物的基本元素是Si,化学性质最不活泼的元素是Ar,气态氢化物的水溶液呈碱性的元素是N.
(2)上述①~⑨元素的最高价氧化物对应的水化物中:碱性最强的物质的化学式为NaOH.
(3)若以元素④和⑤的单质为电极,与元素③的最高价氧化物对应的水化物的水溶液组成原电池,则④的单质在此原电池中作正极(填“正”或“负”)
(4)元素⑦的某氧化物为有刺激性气味的无色气体,其氢化物为有臭鸡蛋气味的无色气体.若这两种气体混合,会生成一种淡黄色粉末.此反应化学方程式为2H2S+SO2=3S↓+2H2O.若此反应中氧化产物的质量为3.2g,则反应中转移的电子数为1.204×1023(填数值).
(5)元素⑧和元素⑨两者核电荷数之差是18,这两种元素中非金属性较弱的元素是溴(填元素名称),能说明这两种元素的非金属性强弱的实验事实是(用离子方程式表示)Cl2+2Br-=2Cl-+Br2.
| 族 周期 | ⅠA | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | 0 |
| 2 | ① | ② | ||||||
| 3 | ③ | ④ | ⑤ | ⑥ | ⑦ | ⑧ | ⑩ | |
| 4 | ⑨ |
(2)上述①~⑨元素的最高价氧化物对应的水化物中:碱性最强的物质的化学式为NaOH.
(3)若以元素④和⑤的单质为电极,与元素③的最高价氧化物对应的水化物的水溶液组成原电池,则④的单质在此原电池中作正极(填“正”或“负”)
(4)元素⑦的某氧化物为有刺激性气味的无色气体,其氢化物为有臭鸡蛋气味的无色气体.若这两种气体混合,会生成一种淡黄色粉末.此反应化学方程式为2H2S+SO2=3S↓+2H2O.若此反应中氧化产物的质量为3.2g,则反应中转移的电子数为1.204×1023(填数值).
(5)元素⑧和元素⑨两者核电荷数之差是18,这两种元素中非金属性较弱的元素是溴(填元素名称),能说明这两种元素的非金属性强弱的实验事实是(用离子方程式表示)Cl2+2Br-=2Cl-+Br2.
6.如图,X、Y、Z、M、N是元素周期表中前四周期中的五种元素,其中M原子的最外层电子数比次外层电子数多4.下列说法不正确的是( )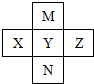
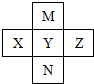
| A. | M形成的氢化物有2种 | |
| B. | M、Y、N的气态氢化物稳定性依次减弱 | |
| C. | X、Y、Z的含氧酸酸性依次增强 | |
| D. | Y的一种氧化物是大气污染物,是形成酸雨的主要物质 |
16.下列关于同分异构体的说法正确的是( )
| A. | 分子式和结构都相同,性质可能相同 | |
| B. | 分子式相同,结构不同,化学性质一定不相同 | |
| C. | 相对分子质量一定相同、官能团一定不同 | |
| D. | 相对分子质量和各元素质量分数一定相同,化学性质不一定相同 |
3.有①Na2CO3溶液 ②NaHCO3溶液 ③NaOH溶液各25mL,物质的量浓度均为0.1mol.L-1,下列说法正确的是( )
| A. | 3种溶液pH的大小顺序是 ③>②>① | |
| B. | 若分别加入25mL0.1mol•L-1盐酸,反应后pH最大的是① | |
| C. | 若将3种溶液稀释相同倍数,pH变化最大的是② | |
| D. | 若3种溶液的pH均为9,则物质的量浓度的大小顺序是③>①>② |
20.在1100℃,一定容积的密闭容器中发生反应:FeO(s)+CO(g)?Fe(s)+CO2(g)△H=a kJ/mol(a>0),该温度下K=0.263,下列有关该反应的说法正确的是( )
| A. | 若生成1 mol Fe,则吸收的热量小于a kJ | |
| B. | 若容器内压强不随时间变化,则可以判断该反应已达到化学平衡状态 | |
| C. | 若升高温度,正反应速率加快,逆反应速率减慢,则化学平衡正向移动 | |
| D. | 达到化学平衡状态时,若c(CO)=0.100 mol/L,则c(CO2)=0.0263 mol/L |